Разработка состава и технологии получения мази, содержащей биокомплекс кобальта с фуразолидоном
Поиск биологически активных веществ, которые надежно и в короткий срок могут подавлять рост инфекционного агента, купировать болевой синдром и адсорбировать экссудат, т.е. обладать выраженным многонаправленным действием, остается в настоящее время актуальной задачей.
В настоящее время инфекционные заболевания имеют большой удельный вес в общей структуре патологии человека. Выделено и идентифицировано более 600 видов микроорганизмов – возбудителей инфекционных процессов различной локализации. Однако во многих случаях лечение и профилактика инфекционных заболеваний продолжает оставаться сложной и трудноразрешимой проблемой в связи с распространением резистентности различных видов микроорганизмов к имеющимся антибактериальным средствам.
В последние годы значительно повысился интерес к использованию лекарственных средств, которые учитывали бы индивидуальные особенности организма больного (и в первую очередь состояние иммунной системы), специфику инфекционного процесса и стадии его развития. Одним из факторов, отягощающих течение инфекционного процесса, является нарушение баланса биометаллов. Известно, что неорганические соли биометаллов не нашли широкого применения в медицине, так как они проявляют относительно низкую биологическую активность и обладают выраженной токсичностью.
Комплексообразование уже известных лекарственных средств с биометаллами является одним из эффективных направлений поиска новых биологически активных соединений, так как оно позволяет сочетать в одном веществе различные виды активности, которые к тому же могут взаимно усиливать друг друга, расширять спектр действия, снижать токсичность лекарственных средств.
Цель работы заключалась в разработке состава и технологии получения мазей, содержащих фуразолидон и его комплексного соединения с кобальтом и в изучении их влияния на антимикробную активность.
Для достижения поставленной цели необходимо было решить следующие задачи:
- изучить антимикробную активность фуразолидона и его комплексного соединения с кобальтом;
- изучить влияние гелевой основы на антимикробные свойства фуразолидона и его комплексного соединения с кобальтом;
- предложить технологию изучения антимикробной мази;
- разработать состав многокомпонентной антимикробной мази для лечения инфицированных ран.
Нами в качестве антимикробного препарата в составе лекарственных форм изучался биокомплекс кобальта с фуразолидоном.
1.1 Профилактика и лечение гнойных ран
«Лечение раны - дело очень сложное, тем более что всякого рода применяемые мероприятия должны соответствовать характеру раны, стадии ее заживления и степени общей реакции организма на полученное повреждение и все его последствия. Недаром количество предложенных методов лечения велико, а количество предложенных средств огромно ...».
Последние три десятилетия основополагающие принципы и традиционные методы лечения гнойных ран подверглись существенному пересмотру. Необходимость этого шага была обусловлена в первую очередь ростом числа гнойно-воспалительных заболеваний и послеоперационных гнойных осложнений, а также ухудшением общих результатов лечения при гнойной хирургической инфекции. Этому способствовали следующие факторы: высокий уровень бытового, производственного и военного травматизма, рост числа иммунодефицитных состояний и формирование антибиотико-резистентных штаммов микроорганизмов. Основным методом комплексной системы лечения больных с гнойно-воспалительными заболеваниями мягких тканей остается на сегодняшний день хирургический. Это, прежде всего, активная хирургическая тактика, к которой относится хирургическая обработка ран. Для повышения клинической эффективности хирургической обработки ран и для улучшения последующего лечения ран широко используются инструментальные методы санации: обработка ран пульсирующей жидкостью, гидропрессивные технологии, т.е. применение сверхвысоконапорного однонаправленного микродисперсного потока жидкости, криовоздействие и криохирургия. Среди физических факторов важное место в лечении ран занимают ультразвуковые (УЗВ) методы санации. Это санация низкочастотным ультразвуковой волной и ультразвуковой волной средней и низкой частоты. Известен способ обработки и лечения ран различными видами лазерного воздействия. Это воздействие углекислым (СО-лазер), гелий-кадмиевым и гелий-неоновым лазерами. Используется и сочетанное применение низкоэнергетических лазерных излучений ультрафиолетового и инфракрасного лазеров. Для лечения ран применяется воздействие электромагнитных излучений низкой интенсивности, а также сочетанное воздействие физических факторов: УЗВ кавитация и лазеротерапия; криовоздействие и лазерное облучение; комплексное воздействие холода, УЗВ и лазера, кислорода, барического давления и магнитного поля. При лечении гнойных ран в настоящее время широко используется вакуумная обработка и вакуум-терапия. Одним из важных элементов местного лечения гнойных ран является дренирование. В настоящее время широко применяются активные методы дренирования: прерывистое активное, постоянное проточное промывание, вакуумное, активное промывное, закрытое аспирационно-промывное, дренирование с использованием гелиевых сорбентов. В лечении ран широко используется и раневой диализ. (16,17,18)
Все перечисленные выше методы относят к механическим и физическим средствам профилактической антисептики, большинство которых не подавляет рост и размножение микробов и не влияет на их биологическую активность. Исключение составляет ультразвуковой метод, который снижает вирулентность микробов, нарушая их способность к адгезии и инвазии. Механические и физические средства антисептики эффективны только в период сосудистых изменений и очищения раны от некротизированных тканей, последующее же их применение может задержать процессы регенерации и эпителизации. Недостатками механической и физической антисептики являются: малая эффективность у больных с иммунодефицитами; высокий риск внедрения в рану микробов из внешней среды или окружающих патологический очаг участков слизистой оболочки или кожи; возможность контаминации удаленными с раны микробами объектов больничной среды; малая доступность, трудоемкость и дороговизна наиболее эффективных средств. (17,19)
Существует различные методики лечения и ведения ран в антибактериальной среде. В настоящее время в лечении гнойных ран широко используются сочетание воздействия физических факторов и лекарственных средств: протеолитических ферментов и диадинамических токов, воздействие СО-лазера и иммобилизированных ферментов протеолиза, лазерной и антиоксидантной терапии, УЗВ и ферментотерапии. В последнее время в лечении гнойных ран нашли применение «высокие технологии», такие как гелиевая и физическая плазмы, плазмотоковая коагуляция, фотоультрозвуковые технологии, фото динамическое воздействие, использование газового потока, содержащего оксид азота (NО-терапия). (20)
В литературе появились сведения о неэффективности и отрицательных воздействиях физических факторов в лечении гнойных ран. Так, при использовании СО-лазера возможно развитие вторичного инфицирования ран, обусловленное изменениями, происходящими в ране после ее обработки лазерным лучом: плотный струп нарушает отток из раны, и, в случае сохранения под струпом инфекции, нагноение неизбежно. Отмечено, что в 12% случаев образуются антибиотикорезистентные штаммы микрофлоры. (19,20)
В комплексном лечении гнойных ран используют антибиотикотерапию, УФО крови, корпоральные и экстракорпоральные методы детоксикации макроорганизма.
Ведущее место в комплексе мер профилактики и лечения раневой инфекции принадлежит антибиотикотерапии. В свою очередь, проводимая без учета характера возбудителя массивная антибиотикотерапия, подавляя нормальную микрофлору и параллельно оказывая общетоксическое влияние на макроорганизм облегчает жизнедеятельность таких антибиотико-резистентных микроорганизмов как синегнойная палочка, протея, анаэробная инфекция.
Широкое распространение устойчивых штаммов возбудителей гнойных инфекций в хирургии ко многим антибиотикам и возможность их эпидемического распространения является серьезной проблемой для построения эффективной антибиотикотерапии. (17,20,21)
Самой основной причиной снижения эффективности антибиотикотерапии гнойных ран является накопление антибиотикорезистентных штаммов в микробной популяции. Это может быть результатом селекции их антибиотика суперинфицирования раны устойчивыми штаммами, а также R-плазмидами, легко передающимися в популяции микроорганизмов за счет различных механизмов генетического обмена. (22)
Особую опасность представляет появление антибиотикозависимых штаммов микроорганизмов, обусловливающее затяжное рецидивирующее течение инфекции с очень низким уровнем развития иммунитета со стороны макроорганизма и даже полным его отсутствием. (21,23,24)
Нарастание антибиотикорезистентности у бактерий - возбудителей раневой инфекции намного опережает сроки широкого внедрения нового антибактериального препарата. Кроме того, тяжелый инфекционный процесс, обусловлен, как правило, ассоциациями Гр.(+) и Гр.(-) бактерий с различной чувствительностью отдельных видов к антимикробным препаратам. Снижение функционального состояния органов выделения под действием инфекционного процесса часто ограничивает возможность применения антибактериальных препаратов в необходимых терапевтических дозах, требующихся для подавления патогенной флоры. (18,24,25)
В настоящее время применение антибиотиков многими исследователями рассматривается, в основном, как средство профилактики раневых осложнений. Лечение гнойно-некротических ран при помощи общей антибиотикотерапии малоэффективно, так как патоморфологические изменения тканей в окружности раны (формирующийся грануляционный вал, нарушения микроциркуляции) не позволяют добиться концентрации антибиотика у раневой поверхности в необходимых терапевтических дозах. (26)
Важное распространение в практической хирургии получила методика лечения ран под повязкой, являющаяся на сегодняшний день основной в клинической практике, так как данная методика проста, удобна и экономически выгодна. Нам представляется более точным определение этого метода как местное медикаментозное лечение ран, так как практически всегда под повязку на рану наносится лекарственное средство в виде растворов, паст и аэрозолей путем электрофореза и другими способами. (27,28)
По разным причинам (обширность поражения, заинтересованность жизненно важных образований) хирургическим путем не всегда удается полностью очистить рану и завершить операцию наложения первичных швов. В таких случаях приходится «готовить» рану к закреплению швами или кожной пластикой, проводя местное медикаментозное лечение, основанное на применении антимикробных лекарственных средств. Если рана небольших размеров (диаметром до 5 см), без выраженных воспалительных изменений и некроза тканей, процессы очищения и регенерации протекают в ней достаточно интенсивно и целесообразно проводить лечение только лекарственными средствами. В таких случаях заживление наступает быстрее (за счет контракции и эпителизации), с хорошими функциональными и косметическими результатами. Местное использование лекарственных средств - наиболее древний способ лечения ран, которому в общей системе терапии ран отводится вспомогательная роль. Однако, вспомогательная роль - это не второстепенная, малозначащая роль. Местное использование лекарственных средств должно дополнять активное хирургическое лечение, хотя и не заменять его. (25,29,30)
В настоящее время в лечении гнойных ран применяется большой арсенал новых лекарственных препаратов и методов. Активно используются электрохимически - активированные растворы, растворы ионов серебра, объемно-заряженная активированная вода, озонированные растворы магнийсодержащий препарат «Поликатан», фитопрепарат «Абсил I»,мед и сахар, милициановое масло, мочевина, фетальные фибробласты, альвеолярные макрофаги, сорбционно-аппликационная терапия, энзимотерапия и пролонгированная энзимотерапия криоспленоперфузия. (30,31)
Важным компонентом местного лечения ран остается использование перевязочных материалов. В последнее время идет активный поиск способов усовершенствования традиционно используемой ватно-марлевой повязки и создание новых перевязочных средств и покрытий с учетом последних достижений в понимании патогенеза раневого процесса на общем фоне развития науки и техники. (26,32,33)
Функции перевязочных средств:
1) предупреждение вторичного попадания в раны микроорганизмов из внешней среды; 2) защита ран от действия дополнительных травматических факторов, холода, жары, избыточного увлажнения или высыхания, от попадания в рану грязи, пыли, слущенного эпителия, других частиц; 3) удаление из раны продуктов распада тканей, микробов, микробных токсинов, ферментов, аллергенов; 4) лечебное воздействие (противомикробное, гемостатическое, обезболивающее, регенерирующее, антиоксидантное, иммуностимулирующее); 5) фиксация защитно-лечебной части перевязочного средства на пораженной части тела, предупреждение смещения и колебания повязки. (22,32,34)
Выполнение столь многочисленных и важных функций возможно, если перевязочные материалы обладают совокупностью свойств: прочностью, пластичностью, антиадгезивностью, проницаемостью для воздуха, паров, патологического субстрата и непроницаемостью для микробов и пыли, сорбционностью, капиллярностью, гидрофобностью. Вполне понятно, что существующие многочисленные современные перевязочные средства, раневые покрытия и ранозаживляющие средства не могут обладать такой совокупностью свойств. (20,35)
Наиболее распространенным методом для лечения ран в настоящее время остается применение мазевых повязок. В ряде клиник для лечения ран до сих пор используют мази с антибиотиками на жировой в основном на вазелин-ланолиновой основе. Эта основа нарушает отток раневого отделяемого, не обеспечивает достаточного высвобождения активного ингредиента из композиции и не способствует проникновению лекарственного вещества внутрь тканей, где находятся микробы, что приводит к переводу острых воспалительных изменений в хронические. В настоящее время практически полностью утратили свою клиническую значимость ихтиоловая мазь и мазь Вишневского. На современном этапе причинами неэффективности лечения гнойных ран вышеуказанными мазями являются наличие антибиотикорезистёнтности микроорганизмов и неправильное использование мазей (наложение повязок в стадии инфильтрации, вызывающее парниковый эффект и способствующее переходу инфильтративно измененных тканей в гнойно-некротические). (15,36,37)
Некоторые недостатки жирорастворимых мазей повторяются в линиментах, маслах и эмульсиях, что ограничивает их использования для лечения ран. В последние десятилетия в клиническую практику для лечения ран внедрены мази на полиэтиленооксидной основе (ПЭО), представляющие комбинацию ПЭО с молекулярной массой 400 и 1500. Последние содержат различные антибиотики и антисептики: левомицетин (левомеколь, левосин); левомицетин, норсульфазол и сульфадиметоксин (левонорсин); диоксидин (5% диоксидиновая мазь, диоксиколь, метилдиоксилин); мафенид ацетат (сульфамеколь, зарубежные аналоги «Сульфамилон», «Наполтан»); йод с поливинилпиролидоном (1% йодопироновая мазь, йодметриксид); метронидазол, левомицетин (метрокаин; зарубежный аналог «Клион»); нитазол, стрептоцид (стрептонитол, нитацид); фурацилин (фурагель); хинифурил (0,5% мазь хинифурила). (24,38)
Для ПЭО-основ гидрофильных мазей характерны выраженная абсорбирующая активность, низкая токсичность, хорошая проницаемость в ткани, пластичность, хорошая растворимость для большинства антибактериальных препаратов, усиление антимикробного эффекта. Мазевая основа ПЭО, обладая осмотической активностью, способствует очищению раны и впитыванию раневых выделений, оказывая потенцирующее действие на лечебный эффект мази в целом. Однако, наряду с положительными свойствами, ПЭО-основам присущи и недостатки: фармакологическая неиндифферентность; раздражающее действие на кожу из-за высокой дегидратирующей способности; несовместимость с некоторыми лекарственными веществами. Нарушение внутриклеточного осмотического равновесия ПЭО-основами из-за высокой дегидратирующей способности ведет к гибели клеток, что в свою очередь может способствовать проникновению химиотерапевтических веществ в системный кровоток и их токсическому действию. Такое действие мазей делает их непригодными для лечения ран в стадии образования и созревания грануляций, и тем более в стадии эпителизации. Наличие в основе твердого и жидкого ПЭО исключает возможность регулировать осмотическую активность за счет изменения соотношения их в пределах более чем 20%, так как при концентрации ПЭО-400 более 80% в основе наблюдается ее разжижение, а при концентрации менее 60% - образование плотной, трудно намазываемой на поверхность кожи системы. Кроме того, поглощение воды сплавом ПЭО составляет лишь 26,3% от взятой навески основы и продолжается не более 14ч. (19,25,39)
Использование в I фазе раневого процесса мазей на гидрофильной основе, к которым относятся и мази на ПЭО, при обильной продукции экссудата в настоящее время во многих случаях малоэффективно. Положение усугубляется и преобладанием среди возбудителей гнойной инфекции устойчивых микроорганизмов к «старым» антибиотикам (левомицетину, диоксидину, стрептоциду), входящим в состав мазей. Проф. Б.М. Даценко, стоявший у истоков изучения влияния на раневой процесс мазей на ПЭО с антибиотиками еще в середине 80-х гг. XX в., когда резистентность микроорганизмов к «старым» антибиотикам была ниже, уже предвидел и не исключал возможности развития резистентности микроорганизмов к антибиотикам, входящим в состав мазей. Это предположение проф. Б.М. Даценко можно подтвердить следующим. По данным исследователей, антибиотикограммы у стафилококков, выделенных при вскрытии гнойных очагов, были чувствительны к левомецитину в 66-69,9%, к стрептомицину в 39,8-47,3% случаев. Выделенные при вторичном инфицировании культуры стафилококков были в 100% случаев устойчивы к стрептомицину. Культуры кишечных палочек, изолированные при вскрытии гнойных очагов, были чувствительны к левомецитину в 15,8-9,3%, а к стрептомицину - в 8,9-4,8%. Штаммы синегнойных палочек и клебсиел, изолированные при вторичном инфицировании, оказались резистентными к левомицетину и стрептомицину. Отмечается устойчивость штаммов стафилококков к тетрациклину в 60-80%, к стрептомицину - в 67-74%, к пенициллину - 97,9%; к левомицетину - 92,6%; к эритромицину - 91,1%. Культура синегнойной палочки устойчива к каномицину в 55,6%, и в 70,8% - к стрептомицину. Протей в 72% случаев устойчив к стрептомицину. Р.С. Суфияров отмечает низкую чувствительность протеев и стафилококков в ассоциации к наиболее широко применяемым в практике «старым» антибиотикам (ампициллину, карбенициллину, эритромицину, линкомицину, ристомицину, левомицетину, тетрациклину), составляющим всего 4%. При этом большинство штаммов протеев и стафилококков, выделенных в монокультуре, оказались резистентными к «старым» антибиотикам: пенициллину, тетрациклину и левомицетину. Известно так же, что и некротические ткани защищают бактерии от воздействия антибиотиков при местном их применении, что является одним из факторов антибиотикорезистентности. Учитывая это, является оправданной разработка иммобилизированных лекарственных форм для лечения ран, содержащих не антибиотики, а антисептики, резистентность микроорганизмов к которым развивается медленнее. (30,40,41)
На сегодняшний день для производства мазей все больший интерес исследователей представляют производные целлюлозы, в частности, натриевая соль карбокси-метилцеллюлозы - Na-КМЦ.
Преимуществами лекарственных форм, содержащих в качестве основы Na-КМЦ, являются следующие:
Лекарственные вещества хорошо и равномерно распределяются в коллоидных растворах Na-КМЦ, так как последние обладают высоким диспергирующим эффектом.
Растворы Na-КМЦ образуют с секретами слизистых гомогенные растворы, что способствует лучшему контактированию лекарственных средств с пораженным участком.
Все мази, приготавливаемые на Na-КМЦ, образуют на коже пленки, легко удаляемые после резорбции лекарственных веществ.
Адсорбционные свойства основ из Na-КМЦ позволяют поглощать кожные экскреторные и секреторные продукты, что особенно важно при наличии экссудата.
5. Применение основы из Na-КМЦ, как и других гидрофильных основ, обеспечивает охлаждение воспаленного участка, вызываемое постепенным испарением воды.
6. Na-КМЦ имеет крутую кривую вязкости в функции концентрации, благодаря чему из нее можно готовить мази любой концентрации, а также линименты и лосьоны.
7. Основа Na-КМЦ относится к «безаллергеновым» вспомогательным веществам.
8. Основа Na-КМЦ значительно более стойка к действию микроорганизмов, чем другие высокомолекулярные углеводы. (26,35,42)
Другая основа - аэросил, относящийся к неорганическим силиконсодержащим полимерам, обладающий большой удельной поверхностью и выраженными адсорбционными свойствами. При наружном применении аэросилсодержащие гели не вызывают раздражения кожи и общетоксического действия. Мази, содержащие аэросил, хорошо удерживаются на коже и обладают пролонгирующим действием. (37,43,44)
В лечении гнойных ран в I фазе применяются также мази с ферментами. «Ируксол», содержащий фермент коллагеназу, «Fibrolan» содержащий фибролизин и «Travase» содержащий смесь протеолитических ферментов. Общим недостатком у этих мазей является сенсибилизирующее действие и кратковременность эффекта в гнойной ране. (25,39,45)
В настоящее время большинство мазей, используемых, в I фазе раневого процесса обладает, узконаправленным действием и не обеспечивают всестороннего влияния на течение раневого процесса. В I фазе раневого процесса необходимо воздействие, как правило, в трех направлениях: усиление оттока, неполитическое действие и подавление микрофлоры.
Для лечения ран в хирургической практике во II фазе раневого процесса широко используются следующие лекарственные препараты: 5-10% метилурациловая мазь; «Винилин»; мазь коланхоэ; солкосериловая мазь и гель; «Пантенол»; актовегин мазь (5%) и актовегин гель (20%). Некоторые из перечисленных лекарственных форм изготавливаются в основном на жировой основе, плохо высвобождающей лекарственные компоненты из композиций, другие очень дорогие. (15,38,46)
Широко применяемые для лечения ран аэрозоли в виде растворов, суспензий, пленкообразующих форм: «Ливиан», «Винизоль», «Лиоксазоль», «Левовинизоль», «Лифузоль» и др. представляют собой либо масляные, либо спиртовые растворы, что не является оптимальным вариантом для лечения гнойных ран. В I фазе раневого процесса, особенно при обильной экссудации, они не должны применяться. Использование их во II фазе раневого процесса ограничено либо недостатками лекарственной формы, либо однонаправленным действием («Лиоксазоль»), либо отсутствием антимикробных средств («Винизоль»). Поэтому эти препараты играют вспомогательную роль в местном лечении ран. Используемые в современной медицине пенообразующие формы аэрозолей содержат различные по действию антимикробные средства антибиотики и антисептики, такие как: диоксизоль (диоксидин), сульйодовизоль (йодовидон), сульйодопирон (йодопирон), нитазол (нитазол), аэрозоль мирамистина, цимезоль (циминаль, тримекаин, порошок окисленной целлюлозы), гипозоль-АН (нитазол, аекол, метилурацил) и другие. Такие формы обладают многокомпонентным действием, что дает возможность использования их для лечения ран в I и II фазе раневого процесса. Не устраивает то, что в состав препаратов входят «старые» антибиотики (левомицетин), к которым развилось привыкание микроорганизмов; другие антимикробные средства (производные йода, мирамистин) оказывают в ране узконаправленное действие на ассоциативную микрофлору, что не отвечает требованиям современной хирургии. Цена некоторых препаратов является также сдерживающей причиной их применения в ЛПУ вследствие недостаточности финансирования. (44,46,47)
Местное медикаментозное лечение ран с использованием существующих лекарственных средств в последние годы становится менее эффективным.
В середине 80-х гг. XX в. на фоне переоценки места и значимости антибиотиков возродился интерес к антисептикам. Все больше исследователей считают, что в лечении и профилактике местных инфекций приоритет должен быть отдан антисептикам или препаратам, в том числе антибиотикам, которые удовлетворяют требованиям, предъявляемым к антисептикам. (40,48,49)
Применение антисептиков при местных и системных инфекционных процессах вызвано рядом целей:
1) предупреждение генерализации процесса;
2) снижение численности популяции и подавление жизнедеятельности находящихся в инфекционном очаге микробов;
3) предупреждение перехода острых местных инфекционных процессов в хроническую форму; в результате суперинфекции, реинфекции и вторичной инфекции, в результате заноса микроорганизмов из внешней среды, с других областей тела больного или в результате активации местной аутофлоры;
4) сохранение нормальной микрофлоры в пораженном органе, а в случае изменения - ее восстановление.
Для профилактической и терапевтической антисептики ран имеется большой выбор антисептиков. (38,49,50)
Однако широко используемые в клинической хирургии растворы перекиси водорода (3%), калия перманганата (0,1-0,5%), борной кислоты (1-3%), диоксидина (1%), хлоргексидина биглюконата (0,02%), фурацилина (1:5000), хлорамина Б (1%), этакридина лактата обладают узким спектром действия, они токсичны и аллергичны. (51)
Традиционно применяемые для обработки гнойных ран водные растворы перекиси водорода и калия перманганата не оказывают существенного влияния. На микробную флору, их антисептический эффект ограничивается раневой поверхностью и не распространяется в глубь тканей, где находятся микробы. Использование раствора перекиси водорода больше отвечает требованию щадящей механической обработки, чем обеззараживанию. Так фурацилин активен в отношении Гр.(+) и некоторых Гр.(-) микроорганизмов, неактивен в отношении синегнойной палочки, протея, энтерококков, токсичен. Рабочие растворы часто контаминированны Гр.(-) микроорганизмами. В отношении хлорамина Б в последние годы отмечено снижение фоновой чувствительности к микроорганизмам и появление устойчивых штаммов микроорганизмов, кроме того хлорамин Б оказывает раздражающее действие на ткани в месте его нанесения. Описаны частые случаи контаминации растворов. Многие исследователи отмечают низкую эффективность фурацилина, хлорамина Б и борной кислоты в отношении стафилококков, кишечной палочки, псевдомонад и протея. Фурацилин и хлорамин Б не эффективны и в отношении Гр.(-) микроорганизмов. Еще меньшую эффективность в отношении Гр.(+) и Гр.(-) флоры оказывают асептол, риванол, йодпирон. Хлоргексидин биглюконат более активен в отношении Гр.(+) микроорганизмов, чем Гр.(-), в популяциях бактерий появляются устойчивые варианты к нему. Эффективность его до 1000 раз снижается в присутствии крови и гноя, а также в кислой среде. Хлоргексидин биглюконат вызывает развитие аллергических реакций у лиц с повышенной чувствительностью кожи. Этакридина лактат оказывает бактерицидное действие на Гр.(+) микроорганизмы, особенно стрептококки. В некоторых микробных популяциях, особенно у стафилококков, широко распространены устойчивые варианты. Рабочие растворы этакридина лактата нередко контаминированны Гр.(-) микроорганизмами. Бализ-2 оказывает бактериостатическое действие на стафилококки, менее активен в отношении протея и псевдомонад. Мирамистин действует на Гр.(+) микроорганизмы хуже, чем на Гр.(-) микроорганизмы. Препараты йода обладают рядом негативных свойств, к ним относятся появление йодоустойчивых штаммов бактерий, снижение антимикробных свойств в присутствии гноя, токсичность, аллергичность, окрашивание кожи вследствие глубокой диффузии в ткани, «узость» лечебной активности. Кроме того, длительное применение мешает заживлению швов и ран. (45,51,52)
В настоящее время отмечается значительное распространение среди больничных и внебольничных штаммов-микроорганизмов биологически устойчивых форм к широко применяемым антисептикам. Например, процент устойчивости у стафилококков к фенолу равен 77,4%, натрия лаурату - 64%, хлорамину Б - 58%, борной кислоте - 65,6%, роккалу - 38,7%, цетилперидиний-хлориду - 31,3%, хлоргексидину - 24,4%. У псевдомонад отмечен высокий процент биологически устойчивых форм к хлоргексидину - 39,9%, хлорамину Б - 30,0%, резорцину - 29,0%, этакридину - 25,1%. Среди энтеробактерий биологически устойчивые формы к этакридину выявлены в 99,5% случаев, к резорцину и йодопирону - 27,0%, хлоргексидину - 9,5%. Не произошло снижения уровня чувствительности в результате адаптации к больничным условиям обитания у стафилококка к декамитоксину, сульфацил-натрию, диоксидину, йодопирону, резорцину, у псевдомонад - к сульфацил-натрию, йодопирону, первомуру, у энтеробактерий - к сульфацил-натрию, диоксидину, хлорамину Б, борной кислоте, а также к этонию, цетилпиридиний-хлориду. К роккалу процент биологически устойчивых штаммов среди внебольничных вариантов энтеробактерий выше, чем среди больничных. Повышение уровня устойчивости бактерий произошло не только к тем антисептикам, к которым они обладали видовой чувствительностью, но и к антисептикам, к которым испытанные виды естественно резистентны. (48,50,53)
А.П. Красильниковым в исследованных выборных штаммах золотистого стафилококка, синегнойной палочки и энтеробактерий выявлены не только биологические, но и клинически устойчивые формы. Видовая устойчивость к рабочим концентрациям антисептиков установлена у псевдомонад и энтеробактерий к цетилпиридиний-хлориду, роккалу, этонию, натрию лаурату и натрию лаурилсульфату, этакридину. Приобретенная клиническая устойчивость выявлена у внебольничных штаммов стафилококка к диоксидину - 71,3% испытанных штаммов, натрию лаурату - 34,0%, этакридину - 15,6%; у псевдомонад к хлоргексидину - 46,8% и хлорамину Б - 2,1%; у энтеробактерий к хлорамину Б- 71,9%, к хлоргексидину - 8,3%. Среди больничных штаммов частота клинически устойчивых форм еще выше. Устойчивые формы стафилококков обнаружены к фенолу (76,3%), борной кислоте (30,5%), хлорамину Б (58%), натрию лаурилсульфату (28,7%). У псевдомонад повысился процент клинически устойчивых штаммов к хлоргексидину, диоксидину, хлорамину Б, у энтеробактерий появились устойчивые штаммы к йодопирону.(54,55)
К 90-м гг. XX в. появились публикации о микробной контаминации почти всех используемых в практике медицины типов антисептиков и обнаружении в них представителей всех систематических групп бактерий и грибов. Основным контаминантом антисептиков являются псевдомонады, часто обнаруживаются условно-патогенные энтеробактерий: клебсиеллы, энтеробактер, серратии и эшерихии. В йодофорах, хлорактивных препаратах, перекиси водорода, фура-цилине обнаруживаются золотистые, эпидермальные и сапрофитные стафилококки.(23,45,56)
Внедряемые в клиническую хирургию антисептики йодофоры, декаметоксин, мирамистин, бетадин, ксимедон, куриозин недоступны в настоящее время для широкого круга населения и ЛПУ из-за чрезмерной цены. (43,56)
Вышесказанное определяет необходимость изыскания экономически выгодных высокоэффективных препаратов для лечения инфекционных заболеваний.
2. ОБЪЕКТЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
2.1 Фуразолидон как антимикробный препарат
N- (5-Нитро-2-фурфурилиден) -З-аминооксазолидон-2
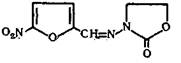
C8H7N3O5M. в. 225,16
Описание. Желтый или зеленовато-желтый порошок без запаха, слабо горького вкуса. Растворимость. Практически нерастворим в воде и эфире, очень мало растворим в 95% спирте.
Подлинность. 0,05 г препарата смешивают с 20 мл воды и 5 мл 30% раствора едкого натра и нагревают; появляется бурое окрашивание.
0,01 г препарата растворяют в 3 мл (плотность не более 0,945); появляется желтое окрашивание. Прибавляют две капли 1 н. раствора едкого кали в 50% спирте; появляется фиолетовое окрашивание, но на смоченных этим раствором стенках .пробирки окраска раствора синяя. 1 мл фиолетового раствора разбавляют водой до 10 мл; появляется желтое окрашивание. После прибавления нескольких капель 1 н. раствора едкого кали в 50% спирте цвет раствора не меняется.
Температура плавления 253-258° (с разложением).
Посторонние вещества. 0,2 г препарата смешивают с 1 мл воды и 0,5 мл разведенной серной кислоты. Смесь нагревают до кипения и осторожно проверяют запах выделившихся паров; не должно появляться ни запаха бензальдегида, ни запаха уксусной кислоты.
Хлориды. 0,5 г препарата смешивают с 25 мл воды при сильном взбалтывании и фильтруют через двойной фильтр. 10 мл прозрачного фильтрата должны выдерживать испытание на хлориды (не более 0,01% в препарате).
Сульфаты. 10 мл того же фильтрата должны выдерживать испытание на сульфаты (не более 0,05% в препарате).
Потеря в: весе при высушивании. Около 0,5 г препарата (точная навеска) сушат при 100-105° до постоянного веса. Потеря в весе не должна превышать 0,5%.
Сульфатная зола и тяжелые металлы. Сульфатная зола из 0,5 г препарата не должна превышать 0,1% и должна выдерживать испытание на тяжелые металлы (не более 0,001% в препарате).
Мышьяк. 0,5 г препарата должны выдерживать испытание на мышьяк (не более б*,0б01% в препарате).
2.2 Количественное определение фуразолидона
Около 0,1 г препарата (точная навеска) помещают в мерную колбу емкостью 50 мл, прибавляют 30 мл диметилформамида (плотность не более 0,945), закрывают колбу притертой пробкой. После растворения препарата прибавляют 2 мл 0,05 н. спиртового раствора едкого кали, перемешивают, охлаждают до 20°, доводят объем раствора диметилформамидом до метки и опять хорошо перемешивают.
0,6 мл раствора помещают в мерную колбу емкостью 100 мл, доводят объем раствора водой до метки и точно через 20 минут, считая с момента прибавления 0,05 н. спиртового раствора едкого кали, определяют оптическую плотность полученного раствора на фотоэлектроколориметре в кювете с толщиной слоя 0.5 см и фиолетовым светофильтром с длиной волны около 360 нм. Во вторую кювету наливают воду.
Во время проведения опытов температура растворов должна быть 20±1°. Место приготовления растворов не должно быть ярко освещено.
Содержание фуразолидона в процентах (X) вычисляют по следующей формуле:
![]()
где D - оптическая плотность испытуемого раствора;
Е1%см - удельный показатель поглощения стандартного образца фуразолидона, определенный в тех же условиях; а - навеска препарата в граммах. Содержание C8H7N3O5 в пересчете на сухое вещество должно быть не менее 98,0% и не более 102,0%.
2.3 Метод диффузии в агар
Применение новых типов мазевых основ требует строго измерять и контролировать активность мазей. В связи с этим уделяется все больше внимания изучению высвобождения лекарственных веществ из мазевых основ в клинических и фармацевтических исследованиях.
В настоящее время имеется много различных методов по определению высвобождения лекарственных веществ мазевыми основами.
Для оценки процесса высвобождения веществ из мазей и определения их антимикробной активности использовали метод диффузии в агар, описанный в ГФ XI издания.
Исследования проводят в асептических условиях. В качестве тест-культур используют: Staphilococcus aureus ATCC 6538-P, Escherichia coli ATCC 25922, Bacillus subtilis ATCC 6633, Bacillus cereus ATCC 10702, Pseudomonas aeruginosa ATCC 9027, Candida albicans ATCC 885-653.
Смесь культур производят стерильным изотоническим растворов натрия хлорида и разводят по стандарту мутности Государственного контрольного института медицинских и биологических препаратов имени Л.А. Тарасевича до образования взвеси с нужной микробной нагрузкой.
Питательную среду (мясо-пептонный агар расплавляют, охлаждают до 40˚ С и вносят в нее