Изоморфизм уравнений диссипативных свойств растворов электролитов
Асеев Д.Г.
Аннотация
Показана принципиальная возможность объединения таких диссипативных свойств, как электропроводность, вязкость и диффузия растворов электролитов.
![]()
На основе этого равенства теоретически получены значения диффузии D, и вязкости растворов электролитов (LiCl, NaCl, KCl) исходя из значений электропроводности, до концентраций насыщенных растворов.
Введение.
Растворы электролитов, в значительной мере определяющие уровень современной химической технологии, продолжают оставаться предметом многочисленных исследований с применением всего арсенала теоретических и экспериментальных методов. Благодаря требованиям практики изучению растворов всегда уделялось и уделяется большое внимание, так как большинство химических реакций, используемых в химической, фармацевтической, пищевой, металлургической и других отраслях промышленности, проходит в растворах.
Все биологические процессы в растительных или животных организмах, в том числе и в организме человека, совершаются в растворах. Это же относится и к процессам, происходящим в почве. Поэтому прогресс таких наук, как биология, медицина, почвоведение и т. д., тесно связан с развитием учения о растворах.
Оптимизация существующих технологий и создание новых требуют в каждом случае сведений о механизмах элементарных процессов, их проявлений в макроскопических неравновесных условиях и т.д.
Огромный экспериментальный материал по свойствам растворов электролитов, накопленный к настоящему времени, нуждается в теоретических обобщениях, удовлетворяющих в той или иной степени, реальным взаимодействиям на микроскопическом уровне.
При этом значительные усилия затрачиваются на исследование индивидуальных характеристик ионов в растворах и их кинетических свойств, называемых иногда транспортными или диссипативными. К последним относят электропроводность, диффузию, вязкость и теплопроводность растворов электролитов.
По очевидным причинам, кинетические свойства определяются преимущественно энергией многочастотных взаимодействий ионов в диэлектрической среде. А это предполагает однозначно привлечение индивидуальных характеристик, как сольватные числа, массы сольватированных ионов, энергии межмолекулярных взаимодействий растворителя, коэффициентов активности, размеров сольватированных ионов. По ряду позиций, экспериментальное определение невозможно в принципе (условие электронейтральности), вероятны лишь теоретические оценки, либо полуэмпирические обработки экспериментального материала на основе ряда правдоподобных, но произвольных по существу, допущений.
Что касается вязкости и диффузии растворов электролитов, то соотношения Эйнштейна, Стокса и Фика дают соответствие с экспериментом лишь в области малых концентраций. Причина – отсутствие приемлемой аппроксимации подвижности ионов и их линейных размеров в условиях сольватации.
Фактический экспериментальный и теоретический материал преимущественно относится к водным разбавленным растворам электролитов. При этом отсутствуют систематические сведения в концентрированных растворах. Наличие широкого спектра методов исследований предопределяет существенную неопределенность при использовании для реальных задач литературных сведений.
Приведенный, далеко не полный перечень сложностей теории растворов электролитов, представляет собой сугубо качественный аспект проблемы системы зарядов в диэлектрических средах.
В последнее время для водных растворов электролитов показана перспективность использования плазмоподобного состояния ионов в растворах, для оценок индивидуальных характеристик от нулевых концентраций до насыщенных водных растворов в удовлетворительном соответствии с экспериментом. Это было достигнуто за счет применения формального аппарата плазмы в более строгом смысле, чем в электростатической теории Дебая – Хюккеля, где понятие плазмы лишь введено в теорию, но нераскрыто по существу.
Принципиальная возможность использования плазменной концепции состояния растворов электролитов отмечена в работах М.М. Балданова (М.М. Балданов. Изв. Вузов. Серия хим. и хим. технология. 1986, т.29, вып. 8, с.38-44 (“Приближение ионной плазмы в теории растворов электролитов”); М.М. Балданов, М.В. Мохосоев. ДАН СССР. 1985, т.284, вып.6, с. 1384-1387 (“Состояние ионов в растворах электролитов в приближении ионной плазмы”))
Основная задача данной работы заключается в определении концентрационных зависимостей диффузии и вязкости растворов электролитов исходя из данных электропроводности полученных экспериментально или теоретически, и сравнении результатов с табличными данными, при постоянной температуре.
Причина подобного подхода к определению диффузии и вязкости кроется в погрешностях экспериментальных определений, например, коэффициент диффузии дается в справочной литературе с погрешность достигающей 15%, вязкость определяется с погрешностью до 5%, а электропроводность определяют довольно с большой точностью, порядка 0,05 – 0,08%.
Объектами исследования было решено выбрать водные растворы хлоридов щелочных металлов: LiCl, NaCl, KCl, поскольку они наиболее изучены и данные по электропроводности, диффузии и вязкости этих растворов наиболее доступны.
Справедливость теоретических моделей и их параметров подтверждаются результатами расчетов. Во всех случаях наблюдается удовлетворительное соответствие оценочных величин с экспериментальными данными в более широком диапазоне изменения концентрации, чем в соответствующих теориях. При этом соблюдается концептуальное единство для всех диссипативных процессов, позволяющее оценивать вязкость и коэффициент диффузии без экспериментальных методов по данным эквивалентной электропроводности, исключая возможность введения тех или иных подгоночных параметров, что имеет теоретический интерес и практическое значение.
2. Современное представление электропроводности растворов
В работах (1 - 6) предложена теоретическая модель многочастотных взаимодействий ионов в растворах электролитов и выведено уравнение электропроводности.
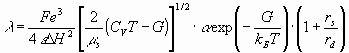 (1)
(1)
Которое получается из двух эквивалентных представлений потока ![]() и
и ![]() . Прировняв по j и выразив получим
. Прировняв по j и выразив получим ![]() .
.
Здесь 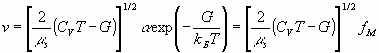 (2)- скорость ионов (fM – максвелловское распределение по скоростям (7)),
(2)- скорость ионов (fM – максвелловское распределение по скоростям (7)),
![]() (3)- напряженность внешнего электрического поля,
(3)- напряженность внешнего электрического поля,
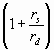 - параметр экранирования учитывающий колебательный характер,
- параметр экранирования учитывающий колебательный характер,
причем 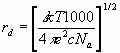 - дибаевский радиус экранирования. Соответствует параметру затухания в гидродинамике.
- дибаевский радиус экранирования. Соответствует параметру затухания в гидродинамике.
Было показано (7), что уравнение (1) справедливо для водных растворов в широком диапазоне концентраций сильных и слабых кислот и оснований, а также солей от 0 до 10 моль/л.
Из выражения (1) видно, что молярная электропроводность раствора зависит от значений диэлектрической проницаемости , энергии межмолекулярных взаимодействий растворителя в жидкой фазе Н, приведенной массы сольватированных ионов электролита s, степени диссоциации , потенциальной энергии ионов в растворах G, определяемых следующими соотношениями:
![]() , (4)
, (4)
![]() , (5)
, (5)
![]() , (6)
, (6)
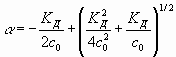 , (7)
, (7)
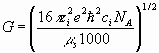 (8)
(8)
где F – число Фарадея; е – заряд электрона; СV=5R/2 – теплоемкость; k – постоянная Больцмана; Т – температура, К; ![]() ,
, ![]() - массы сольватированных ионов, г; М – молекулярная масса растворителя, г; ns – сольватное число иона;
- массы сольватированных ионов, г; М – молекулярная масса растворителя, г; ns – сольватное число иона; ![]() - эффективный радиус молекулы растворителя, см; ri и zi – радиус (см) и заряд иона; rs и rd – радиус сольватированного иона и дебаевский радиус экранирования; р – дипольный момент молекулы растворителя, ед.СГС; КД – константа диссоциации электролита;
- эффективный радиус молекулы растворителя, см; ri и zi – радиус (см) и заряд иона; rs и rd – радиус сольватированного иона и дебаевский радиус экранирования; р – дипольный момент молекулы растворителя, ед.СГС; КД – константа диссоциации электролита; ![]() - постоянная Планка; NA – число Авогадро; - приведенная масса молекулы электролита, г; сi – молярная концентрация ионов (сi= c0); с0 – исходная молярная концентрация электролита.
- постоянная Планка; NA – число Авогадро; - приведенная масса молекулы электролита, г; сi – молярная концентрация ионов (сi= c0); с0 – исходная молярная концентрация электролита.
3. Изоморфизм уравнений
При рассмотрении движения в поле вязких сил удобно ввести понятие подвижности b. Подвижность определяется как предельная скорость, приобретаемая телом под действием силы, равной единице, т. е.
![]()
Таким образом, абсолютная подвижность в системе CGS равна скорости в сантиметрах в секунду, приобретаемой под действием силы в 1 дин. При рассмотрении движения ионов в качестве единицы силы обычно пользуются равным единице градиентом потенциала, действующим на ионный заряд.
Эквивалентная ионная электропроводность , связана простым соотношением с подвижностью. Из определения удельной электропроводности следует, что представляет собой ток, текущий через проводник с равным единице поперечным сечением под действием градиента потенциала, равного единице. Полный ионный заряд в единице объема равен Fc, если с измеряется в эквивалентах на единицу объема. Этот заряд, движущийся со скоростью b’, вызывает ток :
![]() (9)
(9)
или
![]() (10)
(10)
Следовательно, для абсолютной подвижности имеем
![]() (11)
(11)
Для макроскопической частицы, движущейся в идеальной гидродинамической среде, можно вычислить сопротивление трения. Оно выражается через размеры частицы и вязкость среды. Для сферической частицы Стоксом (8) выведена формула
![]() (12)
(12)
где r - радиус сферы. Если ион движется по закону Стокса, его радиус определяется соотношением
![]() (13)
(13)
Если b выражено через предельную эквивалентную электропроводность согласно уравнению (11), то получаем
![]() (14)
(14)
Выразив r в ![]() , а и в обычных единицах, придем к соотношению
, а и в обычных единицах, придем к соотношению
![]() (14а)
(14а)
Движение малых ионов не подчиняется закону Стокса, так как не выполняются необходимые предпосылки. Подвижность связана с коэффициентом диффузии D соотношением
![]() (15)
(15)
где k—постоянная Больцмана. Это ведет к так называемой формуле Эйнштейна — Стокса:
![]() (16)
(16)
Формула Эйнштейна — Стокса справедлива при тех же предположениях, что и уравнение (14).
Связав рассмотренные выше уравнения, через подвижность при условии ее неизменности, получим
![]() (17)
(17)
Сугубо качественно, для произвольного электролита КА в диэлектрической среде имеет место:
![]() (18)
(18)
Причем, k1 и k2 – константы скоростей, ![]() и
и ![]() - сольватированые катион и анион. Очевидно, что при смещении равновесия (18) влево плотность зарядов (равно как и плотность числа частиц) падает, вязкость уменьшается, диффузия увеличивается, электропроводность растет. При смещении равновесия вправо имеет место обратные эффекты. Другими словами, динамика равновесия (18) характеризуется столкновительными инвариантами кинетической теории газов, определяемыми относительными скоростями V смещения ионов в (18) и напряженности внешнего поля E, см. уравнения (2, 3).
- сольватированые катион и анион. Очевидно, что при смещении равновесия (18) влево плотность зарядов (равно как и плотность числа частиц) падает, вязкость уменьшается, диффузия увеличивается, электропроводность растет. При смещении равновесия вправо имеет место обратные эффекты. Другими словами, динамика равновесия (18) характеризуется столкновительными инвариантами кинетической теории газов, определяемыми относительными скоростями V смещения ионов в (18) и напряженности внешнего поля E, см. уравнения (2, 3).
Выражение (2) представляется несколькими вариантами
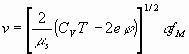 (19)
(19)
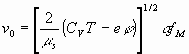 (20)
(20)
Представление скорости (19) отвечает направленному движению зарядов при наличии внешнего поля. Это соответствует явлениям вязкости и электропроводности.
Если же внешнее поле отсутствует (Е = 0), следует уравнение (20) соответствующее диффузии.
Таким образом, для двух возможных значений скоростей по выражениям (19), (20) из уравнения b=V/eE следует:
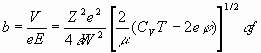 (21)
(21)
 (22)
(22)
Из взаимосвязи (17) выражая коэффициент диффузии и вязкость, через электропроводность, можно теоретически определить эти неточно экспериментально определяемые характеристики раствора.
Взаимосвязь диффузии с электропроводностью была проведена Нернстом и Хартли:
![]() . (23)
. (23)
Где ![]() - средний молярный коэффициент активности.
- средний молярный коэффициент активности.
Предельное значение D при бесконечном разбавлении, когда ![]() , определяется формулой
, определяется формулой
![]() (24)
(24)
было получено Нернстом.
Проверка проводилась, используя эквивалентную электропроводность хлоридов LiCl, NaCl, KCl.
В уравнениях (17) неизвестной величиной является rs – приведенный радиус молекулы АВ, который можно найти, используя уравнение
![]() (25)
(25)
теоретически радиусы иона и сольватированного иона можно оценить по формулам (1-6):
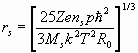 , (26) где
, (26) где
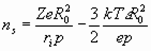 , (27) где
, (27) где
 (28)
(28)
rs – радиус сольватированного иона,
ns – число молекул растворителя окружающих ион,
ri – радиус иона,
Zэ – экранированный заряд ядра,
Z – заряд иона,
I – энергия ионизации,
R0 – радиус молекулы растворителя,
р – дипольный момент молекулы растворителя,
- диэлектрическая проницаемость среды,
Мs – молекулярная масса растворителя.
Zэ – экранированный заряд ядра находится используя константы экранирования Слейтера определяемые по стандартным правилам приводимым в различных учебниках по теоретической основе неорганической химии, в частности (9).
Таблица 1
Радиусы ионов, сольватные числа и радиусы сольватированных ионов рассчитанные по уравнениям 26 – 28
| Ион | I, эв | Zэ |
| ns |
|
| Li+ | 75,62 | 2,7 | 0,5446 | 7,3873 | 4,4246 |
| Na+ | 47,29 | 6,55 | 1,0004 | 3,2301 | 3,3583 |
| K+ | 31,81 | 7,75 | 1,3785 | 1,8682 | 2,7980 |
| Cl- | 3,82 | 4,875 | 1,8100 | 1,0090 | 2,2786 |
Подобные работы: