Особенности сорбционного извлечения палладия (II) из хлоридных растворов волокнами ЦМ-А2, Мтилон-Т и ВАГ
1. Литературный обзор
1.1 Ионообменное равновесие
1.2 Кинетика ионного обмена
1.3 Преимущества волокнистых хелатообразующих сорбентов
1.4 Сорбционное извлечение платиновых металлов
1.4.1 Сорбенты применяемые для извлечения платиновых металлов
1.4.2 Изучение кинетики сорбции палладия на комплексообразующих сорбентах
1.4.3 Формы нахождения палладия в растворе
2. Экспериментальная часть
2.1 Техника безопасности при выполнении работы
2.1.1 Правила работы с едкими веществами (кислоты, щелочи)
2.1.2 Правила безопасной работы с электрооборудованием и электроприборами
2.2 Методика анализа
2.2.1 Спектрофотометрическое определение концентрации палладия с нитрозо-R-солью
2.3 Методики эксперимента
2.3.1 Подготовка волокна
2.3.2 Определение обменной емкости ионита в статических условиях
2.4 Результаты и их обсуждение
2.4.1 Изучение зависимости сорбции палладия на волокнах ЦМ-А2, Мтилон-Т и ВАГ от концентрации металла в равновесном растворе
2.4.2 Расчет термодинамических характеристик процесса сорбции палладия на волокнах ЦМ-А2, Мтилон-Т и ВАГ
2.4.3 Изучение зависимости сорбции палладия на волокнах ЦМ-А2, Мтилон-Т и ВАГ от времени.
2.4.4 Расчет энергии активации процесса сорбции палладия на волокнах ЦМ-А2, Мтилон-Т и ВАГ
2.4.5 Изучение возможности регенерации волокон ЦМ-А2, Мтилон-Т и ВАГ
Выводы
Литература
Приложение 1
Приложение 2
Приложение 3
Приложение 4
Одним из перспективных направлений в комплексном решении экологических проблем является разработка высокоэффективных процессов очистки промышленных газовоздушных выбросов, сточных вод и средств индивидуальной защиты органов дыхания. Важную роль в создании этих процессов играют хемосорбционные волокнистые материалы, обладающие более развитой удельной поверхностью, чем у гранулированных сорбентов, обеспечивающей высокие кинетические параметры процессов сорбции. Изучение механизма сорбции платиновых металлов на ионитах с различными функциональными группами является актуальным и этому вопросу в последнее время уделяется особое внимание.
В литературе есть сообщения об изучении механизма сорбции платиновых металлов на азот и серосодержащих волокнах. Однако публикаций об исследовании механизма сорбции платиновых металлов на комплексообразующих сорбентах сравнительно невелико.
Целью данной работы является изучение особенностей сорбционного извлечения палладия (II) из хлоридных растворов волокнами ЦМ-А2, Мтилон-Т и ВАГ. Определение лимитирующей стадии процесса сорбции палладия волокнами, а так же установление механизма сорбции хлорокомплексов палладия (II) на данных волокнах, влияние температуры и способов регенерации сорбентов.
1.1 Ионообменное равновесие
Ионный обмен - обратимый процесс стехиометрического обмена ионами между двумя контактирующими фазами. Обычно одна из этих фаз ионит, а другая раствор электролита (1).
Если ионит, содержащий только противоионы А, поместить в раствор, содержащий только противоионы В, то ионы А начнут замещаться ионами В из раствора. Через некоторое время установится равновесие: ионит и раствор будут содержать ионы обоих сортов в определенном соотношении. Такое состояние называется ионообменным равновесием(2).
Ионный обмен является обратимой химической реакцией. В соответствии с этим, должно, достигаться состояние равновесия, удовлетворяющее закону действующих масс.
RA + В+ ↔ RB + А+,
где R — матрица ионита с присоединенным к ней фиксированным ионом, А+ и В+ — подвижные ионы(3).
Ионообменное равновесие обусловлено концентрацией раствора, свойствами ионита и обменивающихся ионов, а также температурой. Селективность ионного обмена проявляется в различии абсолютных значений коэффициентов распределения ионов ![]() и
и ![]() , которые для рассматриваемого равновесия можно определить как
, которые для рассматриваемого равновесия можно определить как
![]() и
и ![]() (1),
(1),
где ![]() и
и ![]() - эквивалентные доли ионов А+ и В+ в ионите,
- эквивалентные доли ионов А+ и В+ в ионите, ![]() и
и ![]() - в растворе.
- в растворе.
Деля ![]() на
на ![]() , получим коэффициент селективности, или константу обмена
, получим коэффициент селективности, или константу обмена ![]() , которая, зависит от концентрации обменивающихся ионов:
, которая, зависит от концентрации обменивающихся ионов:
![]() (2).
(2).
Введя поправки на коэффициенты активности ионов в растворе ![]() и
и ![]() , получают уточненный коэффициент селективности
, получают уточненный коэффициент селективности ![]()
![]() (3).
(3).
Следует отметить, что постоянство значений уточненного коэффициента селективности сохраняется только при данной степени замещения. С изменением ![]() величина
величина ![]() изменяется. В таких случаях рассчитывают истинную константу обмена:
изменяется. В таких случаях рассчитывают истинную константу обмена:
![]() (4).
(4).
Поскольку определение ![]() затруднительно, предлагается избрать стандартное состояние ионита в А- и В- формах, в котором
затруднительно, предлагается избрать стандартное состояние ионита в А- и В- формах, в котором ![]() и
и ![]() равны единице.
равны единице.
Истинная константа равновесия обмена разновалентных ионов с зарядами ![]() и
и ![]() выражается уравнением Никольского:
выражается уравнением Никольского:
![]() (5),
(5),
соответствующая взаимодействию эквивалентного числа ионов ионита и раствора:
![]()
На основе теоремы Больцмана Никольский показал, что соотношение коэффициентов активности ионов в твердой фазе не меняется, если свободная энергия их взаимодействия со средой остается постоянной. С известным приближением такое положение справедливо при замещении одного противоиона в ионите на другой, и это позволяет пользоваться для расчета констант обмена уравнением, аналогичным уравнению (3), в котором активности ионов в твердой фазе заменены их концентрациями:
![]() (6),
(6),
где ![]() и
и ![]() - активности катионов с зарядами
- активности катионов с зарядами ![]() и
и ![]() в растворе;
в растворе; ![]() и
и ![]() - концентрации противоионов в твердой фазе, выражаемые в экв на 1 кг или в, мг-экв на 1 г сухого ионита.
- концентрации противоионов в твердой фазе, выражаемые в экв на 1 кг или в, мг-экв на 1 г сухого ионита.
1.2 Кинетика ионного обмена
Стадия, определяющая скорость ионного обмена.
Процесс обмена противоионов включает в себя 5 последовательных стадий:
1. перемещение вытесняющего иона через пленку, окружающую зерно, к его поверхности (пленочная, внешнедиффузионная кинетика);
2. перемещение вытесняющего иона внутри зерна к фиксированным ионам, т. е. к точке обмена (гелевая, внутридиффузионная кинетика);
3. химическую реакцию двойного обмена (химическая кинетика);
4. перемещение вытесняемого иона внутри зерна от точки обмена к поверхности;
5. перемещение вытесняемого иона через пленку, окружающую зерно (3).
Суммарная скорость многостадийного процесса определяется скоростью наиболее медленной стадии. Выявление этой стадии и является первым этапом изучения кинетики ионного обмена (1).
Уравнения, описывающие кинетику ионного обмена.
Проблема распознавания лимитирующей стадии решается на основе фундаментального кинетического анализа ионообменных процессов. Кинетические уравнения имеют сравнительно простой вид, если изменениями состава ионита в результате ионного обмена можно пренебречь.
По результатам анализа рассчитывают степень достижения равновесия ![]() :
:
![]() (7),
(7),
где ![]() - сорбция ионов из раствора за время t;
- сорбция ионов из раствора за время t; ![]() - равновесная сорбция.
- равновесная сорбция.
Если лимитирующей стадией является сам акт обмена ионов, то
![]() (8),
(8),
Величину ![]() вычисляют по уравнению
вычисляют по уравнению
![]() (9),
(9),
где ![]() и
и ![]() — соответственно константы скорости прямой и обратной реакций,
— соответственно константы скорости прямой и обратной реакций, ![]() и
и ![]() — концентрации обменивающихся ионов А+ и В+ в растворе (2).
— концентрации обменивающихся ионов А+ и В+ в растворе (2).
Вывод уравнения для кинетики ионного обмена, лимитирующегося внешней диффузией, был выполнен на основе предположения о постоянстве концентрации раствора и коэффициента распределения адсорбирующегося иона А+ между фазами:
![]() (10),
(10),
Константа скорости диффузии R определяется соотношением
![]() (11),
(11),
где ![]() — коэффициент диффузии через пленку толщиной
— коэффициент диффузии через пленку толщиной ![]() , покрывающую зерно ионита радиусом
, покрывающую зерно ионита радиусом ![]() ,
, ![]() — коэффициент распределения, т. е. отношение концентрации сорбирующегося иона А+ в ионите к концентрации того же иона в растворе в условиях равновесия.
— коэффициент распределения, т. е. отношение концентрации сорбирующегося иона А+ в ионите к концентрации того же иона в растворе в условиях равновесия.
Вывод кинетического уравнения ионообменного процесса, скорость которого лимитируется гелевой диффузией, был сделан для частицы имеющей точно шарообразную форму:
F=1-(6/p2)å(1/n2)exp(-Btn2) (12),
где B=![]() p2/r20 и называется константой скорости гелевой диффузии.
p2/r20 и называется константой скорости гелевой диффузии.
Проверка применимости уравнения (12) сводится к построению графика зависимости Bt от t, который должен быть прямолинейным, если процесс лимитируется гелевой диффузией. Значения Bt удобно определять по экспериментально найденным величинам F с помощью специальной таблицы (Приложение 1). По величине Вτ и известному радиусу зерен смолы можно посчитать среднее значение коэффициента диффузии ![]() (4).
(4).
Методы распознавания плёночной и гелевой диффузии.
Для выяснения механизма кинетики целесообразно работать с проточным раствором(1). Количественное рассмотрение ионного обмена приводит к следующим зависимостям: ln(l –F) = -kt для пленочной кинетики и F=k(t)½ для гелевой кинетики при малых значениях τ (F< 0,05), где k константа. Следовательно, при пленочной кинетике должна получиться прямолинейная зависимость ln(l –F) от t; при гелевой кинетике зависимость F от t½ должна выражаться кривой, которая при малых значениях t имеет прямолинейный ход, а затем искривляется. Построение графических зависимостей на основании экспериментально полученных значений F и t позволяет, таким образом, отличить гелевую кинетику от пленочной. Наличие гелевой кинетики можно также проверить в широкой области, вычислив для каждой пары значений F и t коэффициент взаимодиффузии Di. При этом при всех значениях F и t должно получиться одно и то же значение D. Рассмотренные критерии строго применимы только к изотопному обмену. Сколько-нибудь надежные заключения могут быть получены лишь в том случае, если найденные пары значений согласуются с одним механизмом и не согласуются с другим. Механизм кинетики может быть установлен также на основании данных о зависимости скорости обмена от размера частиц, количества поперечных связей, концентрации раствора и скорости перемешивания, или, соответственно, скорости потока (5).
1.3 Преимущества волокнистых хелатообразующих сорбентов
Волокнистые сорбенты имеют ряд особенностей, связанных с их структурой. Основное преимущество – их высокая удельная поверхность, которая примерно на два порядка выше, чем у гранулированных ионообменников гелевой структуры и в 5-6 раз выше, чем у сорбентов на основе сополимеров пористой структуры(6). Диаметр частиц волокнистых сорбентов на 1-2 порядка меньше среднего размера частиц гранульных сорбентов(7).
Основными характеристиками хелатообразующих сорбентов, в том числе и волокнистых, являются сорбционная ёмкость, кислотно-основные и комплексообразующие свойства, кинетические параметры. Важны так же химическая устойчивость, набухаемость и возможность многократного использования(8).
· Кислотно-основные свойства. Хелатообразующие волокнистые сорбенты, как правило, содержат несколько различных функциональных групп. Это может быть обусловлено неполным превращением реакционно-способных групп промежуточных продуктов при синтезе, гидролизом групп, входящих в состав полимерной матрицы, наличием активных групп в исходном полимере.
· Сорбционные свойства. Величина сорбционной ёмкости волокнистых сорбентов зависит от содержания функциональных групп в сорбенте, природы сорбируемого иона и условий сорбции и изменяется в широком интервале. Высокую сорбционную ёмкость имеют сорбенты с тиоамидными, гидроксамовыми, амидоксимными и др. группами. Эффективность волокнистых сорбентов, особенно при сорбции из разбавленных растворов, можно оценить по величине коэффициентов распределения, достигаемых при их использовании. Для волокнистых сорбентов обычно величины коэффициентов распределения составляют 103-105 мл/г.
· Кинетические свойства. Хорошие кинетические свойства волокнистых сорбентов обусловлены, прежде всего, их высокой удельной поверхностью и хорошей способностью к набуханию. Для характеристики кинетических свойств сорбентов обычно определяют время достижения равновесия при определенном отношении объема анализируемого раствора и массы сорбента (V/m), постоянной температуре и концентрации солевого фона. Также устанавливают скорость, определяющую стадию и определяют эффективные коэффициенты диффузии, используя те же методы, что и при изучении свойств обычных сорбентов.
· Комплексообразующие свойства. Механизм взаимодействия ионов металлов с хелатообразующими сорбентами, в том числе волокнистой структуры, довольно сложен. Основное внимание уделяется выяснению механизма сорбции, состава и структуры образующихся комплексов, а также количественному описанию процесса комплексообразования, который характеризуется величинами констант устойчивости комплексов в фазе сорбента. Для изучения механизма используется ряд методов: элементный анализ, масс-спектроскопия, термогравиметрия, ИК- и ЯГР-спектроскопия.
· Химическая и механическая устойчивость. Для синтеза волокнистых сорбентов применяют различные полимерные материалы, которые в значительной степени определяют их химическую и механическую устойчивость. Химическая устойчивость зависит также от природы введенных функциональных групп.
1.4 Сорбционное извлечение платиновых металлов
1.4.1 Сорбенты, применяемые для извлечения платиновых металлов
К настоящему времени выполнено большое количество работ по извлечению и концентрированию платиновых металлов на различных ионитах. Для изучения механизма сорбции платиновых металлов с различными функциональными группами, исследователями в основном используются такие методы как ИК-спектроскопия, РЭС, дериватография и др.
Сильноосновные аниониты: Палладий (II) прочно удерживается анионитом АВ-17, на основе сополимера стирола и дивинилбензола (8%), содержащий триметиламмонийные активные группы, в Cl-форме. Вымыть палладий (II) можно только 11,5н раствором соляной кислоты, причем процесс элюирования очень длительный. Хорошим элюентом для палладия (II) в этих условиях является раствор 3н хлорной кислоты. Палладий в 1н растворе фтористого водорода хорошо сорбируется анионитом АВ-17 в F-форме. Десорбция палладия (II) из ионита удается лишь концентрированной плавиковой кислотой (20н) (9).
Слабоосновные аниониты: В работе (10) исследован механизм сорбции платины (IV) из солянокислых растворов на сероазотсодержащих сорбентах с моно- и бидентатными функциональными группами. Продукты взаимодействия платины (IV) и сорбентов исследовались методом ИК-спектроскопии. Исследовали три сорбента: слабоосновный анионит с третичной аминогруппой, серосодержащий нейтральный сорбент с сульфидной и третичной аминной группировками:
Сорбент | Функц.гр | %S | %Э | %N | %Э | СОЕ |
| АСП-S-N-1 | CH2S(CH2)2N(C2H5)2 | 8,2 | 2,6 | 3,6 | 2,6 | 1,8 |
| АСП-N-H | CH2N(C2H5)2 | - | - | 4,1 | 2,9 | 2,2 |
| КПП-S-139/7 | CH2SC2H5 | 6,6 | 2,1 | - | - | 0 |
ИК-спектры соединений получали на однолучевом спектрометре ИКС-21 с призмой CsI (220-400 см-1). Образцы готовили в виде суспензии в вазелиновом масле между окнами CsI. Процесс сорбции платины на анионите происходит по ионообменному механизму, а на сероазотсодержащем сорбенте ионообменный механизм усложнен другим процессом – взаимодействием платины с донорным атомом серы. Для выяснения роли атома азота в образовании комплексов платины с сорбентом был использован метод длинноволновой ИК-спектроскопии. Приведены ИК-спектры поглощения области проявления колебаний связи металл-лиганд (200-400 см-1) образцов сорбентов, насыщенных платиной (IV) из солянокислых растворов. В спектре наблюдается интенсивная широкая полоса поглощения с максимумом 315-325 см-1, которую можно отнести к валентному колебанию металл-хлор. В рассматриваемой области интерпритация валентных колебаний связи платина-азот (в случае ее образования при сорбции из солянокислых растворов) затруднена наличием интенсивной полосы νPt-Cl, поскольку известно, что полоса νPt-Nв ИК-спектрах малоинтенсивна.
Позднее (11) была изучена сорбция палладия (II) анионитами на основе стирола и дивинилбензола пористой структуры (АН-511 и АН-406) и анионитом на основе метакрилата и длинноцепочного сшивающего агента - тетравинилового эфира пентаэритрита макросетчатой структуры. Исследования показали, что при переходе к слабокислым средам степень извлечения палладия (II) возрастает до 96%.
Анпилогова Г.Р. с сотрудниками (12) исследовала анионит сетчатой структуры на основе эпихлоргидрина и алифатических полиаминов по отношению к металлам платиновой группы (МПГ). Анионит характеризуется высокими скоростями сорбции МПГ из солянокислых растворов, химической и термической устойчивостью. Для установления механизма сорбции Pt (IV) и Pd (II) анионитом рассмотрены ИК-спектры в дальней области и результаты элементного анализа равновесных продуктов сорбции, полученных в условиях предельного насыщения. Из сильнокислых растворов при комнатной температуре данные металлы извлекаются по анионообменному механизму, при этом взаимодействие оканчивается на стадии образования ионных ассоциатов, о чем свидетельствует соотношение M:N:Cl в продуктах сорбции, а также соответствие значений ν (M-Cl) в ИК спектрах сорбционных комплексов литературным данным для ониевых хлорокомплексов МПГ. Установлено изменение механизма сорбции Pt (IV) и Pd (II) с анионообменного на внутрисферное замещение при переходе от кислых растворов к слабокислым и нейтральным.
В работе (13) изучена адсорбция хлоридных и аммиачных комплексов платины (IV) на синтетических волокнах ВИОН в широком интервале концентраций платины (IV). Показано, что адсорбция комплексных ионов платины (IV) на анионитных волокнах подчиняется уравнению Ленгмюра: изотерма адсорбции на катионитном волокне имеет S-образный вид. Установлено, что адсорбция из растворов аммиаката для всех изученных волокон (АН-1, АН-3 и КН-1) значительно превышает величину адсорбции из кислых растворов. Методом ИК-спектроскопии показано, что координация платины (IV) на волокне АН-1 происходит по атому азота замещенного пиридинового кольца; координация по нитрильной группе не происходит ни на одном из изученных волокон.
Комплексообразующие аниониты: Изучение (14) нового гетероцепного сероазотсодержащего комплексита показало, что он характеризуется высокой химической и термической устойчивостью, высокими величинами сорбционных емкостей по Pd (II). Сорбент проявляет высокую селективность к благородным металлам в присутствии ряда цветных металлов. Методом ИК-спектроскопии установлено, что в слабокислых растворах Pd (II) медленно взаимодействует с вторичными аминогруппами по механизму внутрисферного замещения, а в сильнокислых растворах быстро образует ионные ассоциаты с протонированными аминогруппами с последующим внутрисферным замещением атомов хлора атомами серы диалкилсульфидных групп.
Симанова С.А. с сотрудниками (15) исследовала сорбционные свойства волокнистого сорбента типа Глипан по отношению к хлорокомплексу палладия (II). Установлено, что сорбенты типа Глипан на основе полиакрилонитрила, модифицированные полиэтиленполиаминами (Глипан-А), аминогунидином (Глипан-3) и тиосемикарбазидом (Глипан-1), способны извлекать хлорокомплексы палладия (II) из кислых растворов, а Глипан-А – и из нейтральных. Определены кинетические и емкостные характеристики в солянокислых растворах. При измерении ИК спектров сорбентов в ближней и дальней областях заметны изменения после сорбции хлорокомплекса палладия (II). Показано, что извлечение палладия (II) из кислых растворов волокнами Глипан-А и Глипан-3 происходит по ионообменному механизму с образованием в фазе волокон ониевых хлорокомплексов палладия (II). В случае волокна Глипан-1 сорбция палладия (II) связана с реакциями комплексообразования с функциональными группами сорбента как с полимерным лигандом.
Позже (16) были изучены сорбционные свойства азотсеросодержащего волокна Глипан-1 по отношению к хлорокомплексу платины (II) - K2(PtCl4). Волокнистый сорбент Глипан-1 получали обработкой ПАН волокна тиосемикарбазидом. Волокно содержит группы NH2-NH-C(S)-NH- и карбоксильные группы. Сорбцию проводили в растворах 0,1-4,0 м HCl, 0,1 м KCl, 0,1-1,0 м NaCl (CPt=1-10 ммоль·л-1). ИК спектры сорбентов в области 400-4000 см-1 измеряли на спектрофотометре ИКС-29 с тремя призмами LiF (4000-3000 см-1), CsCl (1800-700см-1), KBr (700-400см-1). Образцы готовили прессованием с KBr. ИК спектры волокон после сорбции в области 140-400 см-1 измеряли на спектрофотометре FIS-3, Hitachi. Образцы готовили прессованием в порошкообразном полиэтилене.
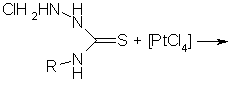 | 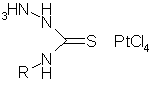 |
В ДИК спектрах волокна после сорбции K2(PtCl4) наблюдается широкий размытый максимум в области 322-326 см-1 и перегиб в области 300 см-1. Было предположено образование в фазе волокна комплекса состава ((RThscH)Pt2+Cl2) цис-конфигурации. Часть тиоамидных групп волокна не участвует в реакции комплексообразования. Высокие скорости извлечения K2(PtCl4) волокном Глипан-1 из кислой среды позволили предположить, что происходит образование ониевых комплексов:
В (17) изучена сорбция Глипан-1 по отношению к хлорокомплексу платины (IV) - K2(PtCl6). На основании совокупности сорбционных характеристик волокна Глипан-1 по отношению к хлоркомплексам Pt (IV) и результатов измерения ДИК спектров предположены основные стадии химических превращений в процессе сорбции. Во всех случаях сорбция связана с реакциями комплексообразования с сорбентом как полимерным лигандом и окислительно-восстановительными превращениями в фазе
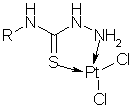 |
волокна. Сорбируемой формой платины оказывается комплекс состава:
Выявлено, что реакции комплексообразования хлорокомплексов платины (II) и платины (IV) с полимерным лигандом, волокном Глипан-1 с привитыми тиосемикарбазидными группами протекают различно.
Авторы работы (18) изучали сорбционные свойства волокна Глипан-А по отношению к хлорокомплексу платины (IV). Данный сорбент получили обработкой ПАН волокна полиэтиленполиамином при повышенной температуре в среде жидкого полиамина. Волокно содержит аминогруппы R-NH2 и R-NH-R´ (СОЕHCl 5.5-6 ммоль·г-1) и карбоксильные группы (СОЕNaOH 1.2 ммоль·г-1). В ДИК спектре волокна Глипан-А после сорбции K2(PtCl6) из кислых растворов наблюдается полоса валентных колебаний Pt-Cl 326-328 см-1. Полосы же валентных колебаний Pt-Cl в соединениях ониевого типа (AH)2(PtCl6) находятся в области 330-340 см-1, а для соединений типа (AH)2(PtCl4) ν (Pt-Cl) располагаются в области 320 см-1. Таким образом, на основании ИК-спектроскопии предположили, что процесс сорбционного извлечения K2(PtCl6) волокном Глипан-А сопровождается частичным восстановлением Pt (IV) до Pt (II). При этом происходит реакция внутримолекулярного окисления-восстановления и в качестве восстановителя выступает хлорид-ион. Т.е. процесс сорбционного извлечения хлорокомплекса Pt (IV) из солянокислых растворов сопровождается образованием в фазе волокна Глипан-А комплексов состава (R2NH2)2(PtCl6) и (R2NH2)2(PtCl4). При сорбции K2(PtCl6) волокном Глипан-А в кислом растворе происходит усложнение контура поглощения ИК-спектра в ближней области (2500-3000 см-1), что свидетельствует об образовании водородных связей между внутрисферными хлорид-ионами и протонами, находящимися во внешней сфере. Изменение контура поглощения полос деформационных колебаний N-H (δ NH) в области 1600 см-1 указывает на возникновение водородных связей. Интересно отметить, что при сорбции K2(PtCl6) волокном Глипан-А из кислых растворов при нагревании (80˚С) в ДИК спектре волокна наблюдаются две размытые полосы валентных колебаний Pt-Cl, которые можно отнести к аминохлорокомплексам Pt(IV) и Pt(II) ((R2NH)2PtCl4) и ((R2NH)2PtCl2) или (R2NH2)((R2NH)PtIVCl5) и (R2NH2)((R2NH)PtIICl3). После сорбции K2(PtCl6) из нейтральных растворов (растворов KCl) волокном Глипан-А не наблюдается заметных изменений в ИК спектрах ни в ближней, ни в дальней областях.
Позже (19) изучены особенности сорбционного извлечения хлорокомплекса платины (II) волокном Глипан-А из солянокислых растворов. Для установления состава комплексов, образующихся в фазе волокна, были сняты ИК спектры в дальней области. Показано, что сорбция K2PtCl4 из кислой среды сопровождается образованием в фазе волокна ониевых соединений типа (R2NH2)2(PtCl4) или (RNH3)2(PtCl4), а из сред, близких к нейтральным – цис-диаминодихлорокомплексов - ((R2NH)2PtCl2) или ((RNH2)2PtCl2). Термогравиметрические исследования образцов волокна Глипан-А с сорбированными на них ионами платины (II) подтвердили результаты спектроскопического исследования.
В статических условиях исследованы (20) сорбционные свойства волокнистых сорбентов, полученных модифицированием полиакрилонитрила полиэтиленполиамином (ГЛИПАН-2), поли-2-метил-5-винилпиридином (ПАН-МВП) и тиосемикарбазидом (ГЛИПАН-1) по отношению к сульфату палладия (II) в 0.1- 5.0 м растворах серной кислоты.
Методами ИК, РФЭ спектроскопии, ЭСП, элементного и дериватографического анализов установлено, что извлечение палладия во всех случаях связано с реакциями комплексообразования с функциональными группами сорбентов. Волокна с азотсодержащими группами отличаются более быстрой кинетикой сорбции. На основании кинетических данных высказано предположение, что вначале происходит образование ониевых соединений с дальнейшим превращением типа андерсоновской перегруппировки и образованием в фазе волокна аминосульфатокомплексов ((RPy)2PdSO4) ((RNH2)2PdSO4), где сульфат-ион выступает в роли бидентантного или мостикового лиганда. Аминосульфатокомплексы палладия (II) прочно удерживаются в фазе волокна (десорбция не превышает 10-15%).
Авторами работы (21) синтезированы гетероцепные полимерные сорбенты, содержащие третичный атом азота. Сорбенты могут быть использованы для концентрирования платиновых металлов. Сорбционным центром является третичный атом азота. Для подтверждения этого проведен элементный анализ образующихся при сорбции комплексов, полученных в разных условиях и выделенных при насыщении сорбента из слабокислых сред. Отношение Me:Cl:N для палладия, золота и платины составляет соответственно 1:2:2, 1:3:1 и 1:6:2. Можно предположить, что из сред, близких к нейтральным, золото и палладий сорбируются с образованием координационно - сольватированных соединений. В случае платины комплексообразование, по-видимому, протекает с образованием ионных ассоциатов, что, вероятно, преобладает при сорбции из кислых сред.
Исследована (22) сорбция родия (III), палладия (II) и платины (IV) из хлоридных растворов полимером на основе полистирола, содержащим диэтилентриаминные группировки. Палладий (II) количественно извлекается из растворов 2-5 М HCl при скорости пропускании раствора до 10 мл/мин на микроколонках с сорбентом объемом 0,1 мл. Родий (III) наиболее эффективно извлекается из 6-7 М HCl, платина (IV) – из 3 М HCl. Методами спектрофотометрии и спектроскопии диффузионного отражения исследованы формы металлов в растворе и твердой фазе. Показано, что при сHCl>1 моль/л сорбция обусловлена ионообменным взаимодействием; извлекаются преимущественно безводные хлорокомплексы металлов. Извлечение металлов на сорбенте при pH>1 сопровождается внутрисферной координацией металлов с азотом функциональных групп. Предложена процедура группового динамического концентрирования родия (III), палладия (II) и платины (IV), заключающаяся в разбавлении пробы до оптимальной концентрации HCl в потоке непосредственно перед колонкой.
Хелатные смолы: В последнее время все большее внимание уделяется использованию хелатных сорбентов для сорбции платиновых металлов (23). Наиболее детально изучена сорбция хлорокомплексов палладия (II) из растворов соляной, серной и хлорной кислот хелатным сорбентом марки ХМС-8-АХ, полученным аминированием хлорметилированного сополимера стирола с дивинилбензолом 8-аминохинолином. Из 1 н раствора соляной кислоты сорбция Pd (II) 100%. Это объясняется тем, что палладий образует прочные хелатные циклы с функциональными группами сорбента.
Исследованы комплексообразующие свойства растворимых ионитов на основе хлормитилированных полистиролов, пиридинкарбоновых кислот и их нитрилов. На основании проведенных исследований найдены оптимальные условия выделения и концентрирования ионов платиновых в частности и палладия (II) из растворов.
Авторами работы (24) был синтезирован новый хелатный сорбент ПВБ-МП-8Т аминированием 3(5)-метилпиразолом хлорметилированного сополимера стирола с дивинилбензолом макропористой структуры. Сорбент представляет собой гранулы сферической формы, окрашенные в бледно-желтый цвет, устойчивые при нагревании в сильнокислых растворах.
Исследована сорбция благородных металлов сорбентом ПВБ-МП-8Т, а также возможности применения сорбента для концентрирования благородных металлов из сложных солевых растворов. Характер взаимодействия сорбента с ионами благородных металлов изучен методом ИК-спектроскопии. ИК-спектры сорбента, насыщенного металлами, исследовали в области 200-4000 см-1. Анализ спектров показал, что полосы поглощения пиразольной группы и полимерной основы прекрываются в области 400-4000 см-1 и существенно не меняются при насыщении сорбента металлом. В области 200-400 см-1 появляются полосы, отнесенные к колебаниям связи Me-N (для Pt-300 см-1), что может свидетельствовать о комплексообразовании благородных металлов по атому азота пиразольнoй группы. Отсутствие в спектрах изменений валентных колебаний группы NH пиразольного цикла при насыщении сорбента металлом позволяет предполагать, что при взаимодействии благородных металлов с сорбентом ионообменные механизм маловероятен.
1.4.2.Изучение кинетики сорбции палладия на комплексообразующих сорбентах
В работе (25) исследовали хлоро- и бромокомплексов Pd двумя типами анионообменных волокон, содержащих третичные амины, на основе п