Кровь как внутренняя среда организма
Кровь как внутренняя среда организма
СОДЕРЖАНИЕ
1. Кровь как внутренняя среда организма
1.1Физиологическое значение крови
1.2Состав крови: плазма и форменные элементы
1.3Физико-химические свойства плазмы
1.4 Белки крови и их значение
1.5 Эритроциты, гемоглобин
1.6 Лейкоциты, их виды и физиологическое значение
1.7 Группы крови и резус-фактор
1.8 Переливание крови. Кровезаменители
1.9 Свертывание крови: свертывающая и противосвертывающая системы
1.10 Фибринолиз1
1.11 Кроветворение и регуляция системы крови
1.12 Образование лимфы и ее роль
Список использованных источников
кровь физиологическая плазма лимфа
1. Кровь как внутренняя среда организма
1.1 Основные функции крови
1. Дыхательная - доставка клеткам кислорода и удаление углекислого газа.
2. Трофическая (питательная) - кровь обеспечивает клетки питательными (глюкоза, аминокислоты, жиры) веществами, водой, витаминами, минеральными веществами.
3. Экскреторная - удаление от клеток конечных продуктов метаболизма.
4. Терморегуляторная - кровь обеспечивает стабилизацию температурных условий для клетки путем транспорта тепловой энергии, образующейся в активно функционирующих клетках.
5. Защитная функция крови направлена на предотвращение критических для клетки подъёмов в крови концентрации экзогенных токсических веществ и ядов путём неспецифической адсорбции их на поверхности клеток крови и образованием комплексов с белками плазмы с последующим выведением их из организма органами выделения. Лейкоциты удаляют из организма генетически чужеродные соединения биологического происхождения путём фагоцитоза, цитолиза, гидролиза или образованием специфических антител в реакциях гуморального и клеточного иммунитета.
6. Гомеостатическая роль крови заключается в стабилизации важных констант организма (концентрации водородных ионов-рН, осмотического давления, ионного состава тканей).
7. Кровь обеспечивает водно-солевой обмен клеток.
8. Циркулирующая кровь обеспечивает связь между органами -важное условие гуморальной регуляции функций в организме. Кровь переносит гормоны и другие биологически активные вещества от мест образования к клеткам-мишеням.
9. Транспортная является следствием функционирования миокарда как насоса, энергия сокращения которого обеспечивает перемещение крови по сосудистой системе организма и её контакт со всеми анатомо-функциональными системами организма.
10. Белки плазмы могут быть использованы организмом в качестве источника аминокислот.
Кровь обладает способностью к свертыванию, что предотвращает опасные для жизни кровопотери при повреждениях тканей и кровеносных сосудов.
Общее количество крови в организме взрослого человека составляет 6 - 8% от массы тела, или приблизительно 4,5 - 6 л. Массивная кровопотеря около 1/3 её объёма (примерно 1,5 л) сопровождается падением артериального давления и последующей гибелью организма.
1.2 Состав крови: плазма и форменные элементы
Стабилизированная антикоагулянтом, кровь в пробирке разделяется на осадок - форменные элементы (эритроциты, лейкоциты, тромбоциты) и плазму. Плазма - прозрачная жидкость желтоватого цвета. При свёртывании крови вне организма (коагуляция крови) образуются кровяной сгусток, включающий форменные элементы и фибрин, и сыворотка. От плазмы сыворотка отличается, прежде всего, отсутствием фибриногена.
Плазма, состав плазмы крови, значение белков плазмы
Плазма крови на 90 - 92% состоит из воды, 7 - 8% плазмы составляют белки (альбумины - 4,5%, глобулины - 2 - 3%, фибриноген - до 0,5%), остальное количество сухого остатка приходится на питательные, минеральные вещества и витамины. Общее содержание минеральных веществ приблизительно равняется 0,9%. Условно выделяют макро- и микроэлементы. Границей является концентрация вещества 1мг%. Макроэлементы (натрий, калий, кальций, магний, фосфор) прежде всего обеспечивают осмотическое давление крови и необходимы для жизненно важных процессов: натрий и калий - для процессов возбуждения, кальций - свертывания крови, мышечных сокращений, секреции; микроэлементы (медь, железо, кобальт, йод) рассматриваются как компоненты биологически активных веществ, активаторы ферментативных систем, стимуляторы гемопоэза, метаболизма.
1.3 Физико-химические свойства плазмы
Онкотическое и осмотическое давление - сила, с которой молекулы органического и неорганичеcкого вещества притягивают к себе молекулу воды для создания водной оболочки. Осмотическое давление создают вещества неорганической природы, онкотическое - органической.
При общем осмотическом давлении плазмы 7,6 атм, онкотическое давление равно 0,03-0,04 атм (25-30 мм рт. ст.). Крупномолекулярные белки не проникают в интерстициальное пространство из сосудистого русла и являются фактором, определяющим обратный ток воды из межклеточного пространства в венулярном отделе микроциркуляторного русла. Осмотическое и онкотическое давление определяют объемное распределение воды между клеткой и внеклеточным пространством. Вода перемещается через мембрану в сторону более высокого осмотического давления. По величине осмотического давления (основная роль в поддержании которого на 80% принадлежит NaCl, на 15% глюкозе и на 5% мочевине) относительно плазмы все растворы можно разделить на:
1. Изотонические - равные по осмотическому давлению (0,9% раствор NaCl).
2. Гипотонические - с более низким по отношению к плазме осмотическим давлением.
3. Гипертонические - с превышающим осмотическое давление плазмы. Все инъекционные растворы должны быть изотоничными клетке, иначе могут вызвать или потерю воды клеткой (гипертонические растворы), или поступление воды в клетку с последующим ее набуханием и разрывом мембраны (гипотонические растворы).
Кислотно-основное состояние крови. Буферные системы. Алкалоз и ацидоз
Кислотно-основное состояние крови зависит от концентрации в среде ионов водорода, которое выражается в единицах рН . Концентрация водородных ионов (рН = -lg ( Н+) на уровне 7,37 - 7,43 для артериальной крови является жёсткой константой организма. рН венозной крови в связи с более высокой концентрацией углекислого газа и органических кислот ниже и снижается до 7,30 - 7,35, внутриклеточный рН равняется 7,26 - 7,30. Повышение концентрации водородных ионов (снижение рН) определяется как ацидоз, а снижение концентрации протонов обозначается как алкалоз. Сохранение постоянства рН крови обеспечивается физико-химическими буферными системами и функционированием физиологических систем организма - выделительной и дыхания.
![]() (1)
(1)
Любая буферная система состоит из равновесного соотношения протонов (Н+), сопряжённого основания (А-) и недиссоциированной слабой кислоты: В соответствии с законом действующих масс повышение содержания протонов сопровождается увеличением концентрации недиссоциированной кислоты, а ощелачивание среды приводит к росту диссоциации кислоты с образованием протонов, и константа диссоциации (равновесия) К не изменяется.
Физико-химические буферные системы крови
1. Буферная система гемоглобина является наиболее мощной. Эта система функционирует благодаря тому, что белок глобин в молекуле гемоглобина обладает амфотерными свойствами, оксигемоглобин является более сильной кислотой, чем дезоксигемоглобин (восстановленный гемоглобин). В тканях гемоглобин играет роль щёлочи, в лёгких же ведёт себя как кислота, предотвращая защелачивание крови после выделения из неё углекислоты.
2. Карбонатная буферная система представлена слабой угольной кислотой (Н2СО3) и слабым основанием (NaHCO3-). При поступлении в кровь более сильной, чем угольная, кислоты происходит обмен ионами натрия с образованием слабодиссоциирующей и легкорастворимой угольной кислоты, её избыток снижается при выделении лёгкими углекислого газа.
3. Фосфатная буферная система образована дигидрофосфатом и гидрофосфатом натрия: NаН2РО4/Nа2НРО4. При поступлении в кровь кислоты она реагирует с гидрофосфатом с образованием дигидрофосфата, щёлочь реагирует с дигидрофосфатом натрия, образуя гидрофосфат. В обоих случаях избытки образующихся гидро- или дигидрофосфатов удаляется из организма почками.
4. Белки плазмы играют роль буферной системы благодаря амфотерным свойствам, которые обусловлены амино- и карбоксильной группами: в кислой среде белки ведут себя как щёлочи, связывая кислоты, в щелочной - как кислоты.
Роль функциональных систем. Помимо буферных систем, обеспечивающих базовый уровень регуляции реакции крови, система поддержания рН включает функциональные системы, благодаря которым происходит регенерация буферов.
1. Дыхательная система обеспечивает выделение из организма летучего ангидрида угольной кислоты - углекислого газа.
2. Почки удаляют из организма избыток кислот и оснований. При ацидозе возрастает выделение дигидрофосфата натрия NaН2РО4, при алкалозе - гидрофосфата натрия и NаНСО3, соответственно изменяется кислотность мочи, рН которой колеблется в широком диапазоне (4,5 - 8,5).
3. Важную роль в поддержании рН крови играет желудочно-кишечный тракт, слизистые оболочки которого секретируют эквимолярные количества соляной кислоты (желудок) и гидрокарбоната (кишечник и поджелудочная железа). При патологии состояния, сопровождающиеся неукротимой рвотой, способны привести к алкалозу за счет потери ионов водорода, а поносы, сопровождающиеся потерей бикарбонатов, - к системному ацидозу.
4. Кроме того, в организме функционирует система метаболической нейтрализации - связывания кислых продуктов в процессе аммониогенеза и цикла Карно в печени и почках; а также удаления щелочных валентностей за счет образования молочной кислоты в мышцах.
1.4 Белки крови и их значение
1. Обеспечивают онкотическое давление плазмы.
2. Обеспечивают вязкость плазмы, что имеет значение в поддержании артериального давления крови. Вязкость плазмы по отношению к вязкости воды равна 2,2 (1,9-2,6).
3. Белки плазмы играют питательную функцию, являяcь источником аминокислот для клеток (в 3л плазмы содержится около 200 г белков, которые обновляются за 5 суток примерно на 50%).
4. Служат переносчиками гормонов, являются транспортной формой микроэлементов, могут связывать катионы плазмы, препятствуя их потере из организма.
5. Принимают участие в свёртывании крови, являются обязательным компонентом иммунной системы организма, обеспечивают взвешенное состояние эритроцитов, играют роль в поддержании кислотно-основного состояния крови.
Белки плазмы методом электрофореза могут быть разделены на 3 группы: альбумины, глобулины и фибриноген; фракция глобулинов разделяется на альфа-1, альфа-2, бета и гамма-глобулины. Альбумины составляют 60% всех белков плазмы, благодаря низкому молекулярному весу (69000 Д) обеспечивают на 80% онкотическое давление. Благодаря большой суммарной площади поверхности, выполняют роль переносчика многих эндогенных (билирубин, желчные кислоты, соли желчных кислот) и экзогенных веществ. Глобулины образуют комплексные соединения с углеводами, липидами, полисахаридами, связывают гормоны, микроэлементы. Фракция гамма-глобулинов включает иммуноглобулины, агглютинины, многие факторы системы свертывания крови. Фибриноген является источником фибрина, который обеспечивает образования сгустка крови.
1.5 Эритроциты, гемоглобин
Эритроциты - безъядерные клетки, основной функцией которых является обеспечение газообмена. 95% массы эритроцитов составляет гемоглобин. Содержание эритроцитов в периферической крови колеблется около 5 млн в 1 мкл. У женщин содержание эритроцитов примерно на 10% ниже, чем у мужчин. Размеры эритроцитов: диаметр 7-8 мкм, объём 85-90 мкм3, площадь поверхности 145 мкм2. Основным источником энергии в эритроцитах является глюкоза, которая на 90% окисляется в ходе анаэробного гликолиза. Энергия расходуется на восстановление текучести мембраны, остаточной деформации, работу ионных насосов, синтез глютатиона в реакциях восстановления, защищающих эритроциты от окислительной денатурации. Синтезируемый в эритроцитах 2,3-дифосфоглицерат (2,3-ДФГ) регулирует (уменьшает) сродство гемоглобина к кислороду, что ускоряет процесс отдачи кислорода. Продолжительность жизни эритроцита 60-90, максимально 120 дней. Разрушение происходит, в основном, макрофагами селезёнки и костного мозга, купферовскими клетками печени (внутриклеточный, внесосудистый гемолиз). После отщепления от гемоглобина гем превращается в желчный пигмент билирубин и поступает в кишечник. Частично всасывается, частично выводится из организма в виде стеркобилина (кал) и уробилина (моча). Железо используется для повторного синтеза гемоглобина. Гемоглобин связывается в крови с белком гаптоглобином, этот комплекс в дальнейшем фагоцитируется купферовскими клетками печени.
Подсчет числа эритроцитов.
Кровь разводится 3% раствором хлорида натрия в 200 раз. Заполняется камера Горяева, под микроскопом подсчитывают число эритроцитов в 5 больших квадратах, расположенных по диагонали счетной камеры. Расчет по формуле :
![]() (2).
(2).
X - число эритроцитов;
А - число эритроцитов в 5 больших квадратах (= 80 маленьких);
200 - разведение;
1/4000 мм3 - объём части камеры над 1 маленьким квадратиком;
А/80 - среднее арифметическое число эритроцитов в маленьком квадрате.
Гемоглобин.
Гемоглобин - хромопротеид, окрашенный в красный цвет после присоединения к Fe++ кислорода. Состоит из белка глобина и простетической группы гема. В молекуле гемоглобина содержится одна молекула глобина и четыре молекулы гема. Гем имеет в своем составе атом двухвалентного железа, способный присоединить и отдать молекулу кислорода. Одна молекула гемоглобина присоединяет четыре молекулы кислорода. 1 гр гемоглобина присоединяет 1,34 мл кислорода. Содержание гемоглобина у мужчин 16,6 г в 100 мл крови (166 г/л), у женщин - 130 г/л.
Значение гемоглобина:
1) Выполняет роль переносчика О2 от лёгких к тканям.
2) Участвует в транспорте СО2 от клеток к лёгким.
3) Составляет гемоглобинную буферную систему и регулирует кислотно-основное состояние крови.
Виды гемоглобина
В период внутриутробного развития зародыша (7-12 недель) эритроциты содержат примитивный гемоглобин (HbP), на 9-й неделе появляется гемоглобин фетальный HbF, а перед рождением - гемоглобин взрослых (HbА). Фетальный гемоглобин в течение первого года жизни ребенка полностью заменяется на HbА. Примитивный и фетальный гемоглобины обладают более высоким сродством к кислороду, что обеспечивает его насыщение кислородом при более низком парциальном давлении.
Соединения гемоглобина
В норме гемоглобин содержится в виде нескольких соединений:
1) Восстановленный, или дезоксигемоглобин (Hb). Имеет 4 свободных связи, к которым могут присоединяться лиганды - кислород, угарный газ.
2) Оксигемоглобин (HbО2). Образуется из восстановленного гемоглобина присоединением кислорода.
3) Карбгемоглобин (HbСО2). Образуется в тканях после присоединения к гемоглобину углекислого газа.
Примерно 8-9% гемоглобина в крови находится в виде соединения метгемоглобин (MetHb). Метгемоглобин образуется в результате взаимодействия со свободными радикалами. Железо в метгемоглобине находится в трехвалентной форме, поэтому метгемоглобин не способен взаимодействовать с кислородом.
При отравлениях угарным газом образуется карбоксигемоглобин (HbСО). Обладает высоким сродством к кислороду, поэтому при небольших концентрациях угарного газа в крови гемоглобин блокируется и теряет способность транспортировать кислород.
Определение содержания гемоглобина в крови
Пипеткой набирают 20 мм3 крови и смешивают с 0,1 нормальным раствором соляной кислоты, налитым в среднюю пробирку гемометра Сали. После образования солянокислого гематина - соединения, имеющего интенсивный коричневый цвет, в пробирку по каплям прибавляют дистиллированную воду до уравновешивания цвета раствора в средней пробирке с цветом эталонных растворов. По нанесенной на пробирку шкале по уровню полученного раствора определяют концентрацию гемоглобина.
Гемолиз эритроцитов, виды гемолиза.
Гемолиз - это массивное внутрисосудистое разрушение эритроцитов с выходом свободного гемоглобина в плазму. Гемоглобин начинает выделяться почками, что повреждает нефрон. Виды гемолиза:
1. Осмотический.
2. Химический.
3. Механический.
4. Термический.
5. Биологический.
Причины гемолиза в организме:
1. Переливание несовместимой крови.
2. Сепсис, влияние гемолитических микроорганизмов.
3. Попадание в организм гемолитических ядов.
4. Отравление различными органическими и минеральными веществами.
Опасность гемолиза заключается в развитии комбинированного шока, а в последующем - острой и хронической почечной недостаточности.
Скорость оседания эритроцитов.
При стоянии крови, не свёртывающейся вследствие добавления антикоагулянтов, наблюдается оседание эритроцитов. СОЭ в норме равна у мужчин 1-10 мм/ч, у женщин - 2-15 мм/ч. На СОЭ влияют главным образом свойства плазмы (содержание крупномолекулярных белков - фибриногена и глобулинов), а также размеры и форма эритроцитов. При воспалительных и онкологических заболеваниях скорость оседания эритроцитов возрастает в связи с повышенной способностью эритроцитов образовывать агрегаты. На скорость оседания эритроцитов влияет белковый состав плазмы. СОЭ уменьшается при увеличении содержания альбуминов и возрастает при увеличении концентрации фибриногена, гаптоглобина, липопротеидов, иммуноглобулинов.
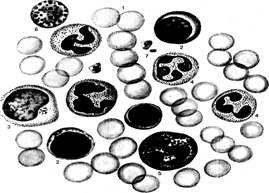
Рис. Клетки периферической крови человека.
1 – эритроциты, 2- лимфоциты, 3- моноциты, 4 – нейтрофильные гранулоциты, 5 – эозинофильные гранулоциты, 6 – базофильные гранулоциты, 7 – тромбоциты.
1.6 Лейкоциты, их виды и физиологическое значение
Лейкоциты содержатся в периферической крови в концентрации 4-9 ´ 109 /л. Увеличение количества лейкоцитов называется лейкоцитозом, снижение - лейкопенией. Причиной лейкопении являются токсические и радиационные воздействия на организм. Лейкоцитоз может развиваться у здорового человека при мышечной работе, во время сильных эмоций, после приёма пищи, у женщин при беременности. Патологический лейкоцитоз характерен для инфекционных и воспалительных заболеваний и обеспечивает повышение реактивности организма. Определение числа лейкоцитов имеет большое диагностическое заболевание.
Группы лейкоцитов:
1. Зернистые (гранулоциты). Содержат специфическую зернистость в цитоплазме.
2. Незернистые (агранулоциты). Не содержат зернистости в цитоплазме.
Гранулоциты - клетки диаметром 7-10 мкм подразделяются на:
а) Эозинофилы. Зернистость окрашивается кислыми красителями. Обезвреживают и разрушают токсины белкового происхождения, комплексы антиген-антитело, фагоцитируют гранулы базофилов и тучных клеток, продуцируют гистаминазу, разрушающую гистамин. Количество увеличивается при аллергических реакциях, глистных инвазиях, интоксикациях;
б) Базофилы. Зернистость окрашивается основными красителями, крупная, в цитоплазме - гранулы, содержащие гистамин и гепарин. Благодаря секреции гистамина и гепарина базофилы способствуют миграции нейтрофилов. Базофилы способствуют так же рассасыванию погибших тканей и заживлению. Мембрана базофилов имеет рецепторы к иммуноглобулину Е, который комплементарен к иммунному комплексу, в составе которого есть этот глобулин. После гидролиза лизосомальными ферментами в цитоплазме базофила иммунного комплекса, рецептор вновь синтезируется и через 12 - 24 часа транслоцируется на поверхность мембраны. Благодаря таким циклам, базофил способен элиминировать из плазмы большое количество антигенов, блокированных иммуноглобулином Е.
в) Нейтрофилы имеют мелкую зернистость, которая окрашивается нейтральными красителями. По форме ядра и зрелости делятся на:
- юные (метамиелоциты) - ядро рыхлое, бобовидное,
- палочкоядерные - ядро в виде изогнутой палочки, подковки или буквы S,
- сегментоядерные - ядро состоит из 2-3 долек, связанных между собой тонкими перемычками. Это зрелые нейтрофилы.
Нейтрофилы - микрофаги - фагоцитируют, переваривают и уничтожают микробов, обладают противовирусным действием (продуцируют интерферон). Метаболической особенностью нейтрофилов является анаэробный гликолиз, поэтому нейтрофилы способны осуществлять фагоцитоз в разрушенных и размозженных тканях с ограниченной оксигенацией.
Агранулоциты не содержат зернистости.
а) Лимфоциты - клетки размером 4,5 - 10 мкм ( подразделяются на малые, средние, большие). Содержат очень плотное, темное ядро, цитоплазма окружает ядро в виде узкой каймы, окрашивается в голубой или синий цвет основными красителями.
По функции и месту созревания лимфоцитов различают:
- Т-лимфоциты - дифференцируются в тимусе. Участвуют в клеточном иммунитете.
- В-лимфоциты - дифференцируются в костном мозге. Синтезируют антитела и участвуют в гуморальном иммунитете.
б) Моноциты имеют размеры 10-12 мкм, ядро - бобовидное, подковообразное, дольчатое, цитоплазма окружает ядро более широкой полосой, светло-голубая. Являются тканевыми макрофагами. Завершают процесс фагоцитоза в очагах воспаления, фагоцитируют и собственные поврежденные ткани. Способствуют восстановлению, регенерации.
Лейкоцитарная формула - это процентное соотношение всех видов лейкоцитов. Лейкоцитарная формула, наряду с изучением изменений числа лейкоцитов имеет диагностическое значение.
Гранулоциты | Агранулоциты | ||||||
| Базофилы | Эозинофилы | Нейтрофилы | Лимфоциты | Моноциты | |||
| миелоциты | юные | палочкоядерные | сегментоядерные | ||||
| 0-1% | 1-5% | 0% | 0-1% | 1-5% | 45-70% | 20-40% | 2-10% |
Ядерный сдвиг лейкоцитарной формулы влево - увеличение молодых форм и появление в периферической крови незрелых клеток (миелоциты, промиелоциты). Увеличение сегментоядерных форм при снижении более молодых называется ядерный сдвиг вправо. Сдвиг влево отражает высокие потенциальные возможности костного мозга в отношении продукции лейкоцитов и является хорошим прогностическим признаком при заболеваниях.
Подсчет числа лейкоцитов.
Кровь разводится в 20 раз 5% раствором уксусной кислоты, подкрашенной метиленовой синью. Заполняют камеру Горяева и под микроскопом подсчитывают число лейкоцитов в 25 больших (400 маленьких) квадратах. Расчет числа лейкоцитов в 1 мкл производится по формуле:
![]()
где Х - число лейкоцитов искомое,
В - число лейкоцитов в 25 больших квадратах.
Тромбоциты и их роль в организме.
Тромбоциты имеют дисковидную форму диаметром от 2 до 5 мкм, толщиной около 0,5 мкм. В крови содержится 180-320 х 109 /л. Образуются в костном мозге.
Значение тромбоцитов в организме:
1) Участвуют в гемостазе (содержат тромбоцитарные факторы свёртывания).
2) Участвуют в транспорте креаторных веществ, важных для сохранения сосудистой стенки, стимулируют восстановление эндотелия.
3) Возможно, фагоцитируют низкомолекулярные соединения.
Мембрана тромбоцитов содержит рецепторы, необходимые для активации тромбоцитов, их адгезии (приклеиванию к субэндотелию) и агрегации. Мембрана содержит фосфолипидный фактор 3, формирующий активные коагуляционные комплексы с плазменными факторами свертывания крови. В мембрану встроены гликопротеины, ответственные за адгезию тромбоцитов к коллагену, имеются рецепторы к фактору Виллебранда. Гранулы цитоплазмы содержат АТФ, кальций, серотонин, катехоламины. Кальций регулирует адгезию, образование тромбоксана А2, АДФ, способствует агрегации. Серотонин и катехоламины обеспечивают сокращение сосудов в местах их повреждений.
1.7 Группы крови, резус-фактор
Проблема групповой принадлежности крови была решена исследованиями К. Ландштейнера и Я. Янского, что позволило широко применить в практической медицине переливание крови. Было установлено, что мембрана эритроцитов человека является носителем более 300 антигенов, обладающих способностью вызывать против себя образование иммунных антител. Система антигенов эритроцитов АВО отличается от других групп крови тем, что содержит в сыворотке крови естественные анти-А (альфа) и анти-В (бета) антитела-агглютинины. Антитела не вырабатываются против "своего", т.е. присутствующего в эритроците данного человека антигена - А, В, и Н. Однако антигены А и В широко распространены в животном мире, поэтому после рождения человека в его организме начинается формирование антител против антигенов А и В, поступающих с пищей, бактериями. В результате в плазме появляются анти-А и анти-В антитела, максимум активности их продукции приходится на 8 - 10 летний возраст. Эти антитела называются изоантителами, или агглютининами, поскольку они вызывают склеивание (агглютинацию) эритроцитов, содержащих на мембране соответствующие антигены (агглютиногены).
Группы крови определяют путем постановки реакции агглютинации крови реципиента (человека, которому переливают кровь) со стандартными сыворотками I-IV групп крови, полученных от доноров. Варианты возможных результатов реакций представлены в таблице:
- отсутвие реакции несовместимости при переливании крови донора
| Группа сыворотки (реципиента) | Группа эритроцитов (донора) | |||
| I (0) | II (А) | III (В) | IV(АВ) | |
| I (a и b) | - | + | + | + |
| II (b) | - | - | + | + |
| III (a) | - | + | - | + |
| IV (0) | - | - | - | - |
Подобные работы: