Технология производства полиакрилонитрила
Технология производства полиакрилонитрила
Полимер нитрила акриловой кислоты (полиакрилонитрил) был впервые получен Моро в 1893 г. из этиленциангидрина и амида акриловой кислоты. Затем в 1931 г. Карозерс разработал метод получения латексов из полиакрилонитрила. Позднее, в 1940 году был предложен метод сополимеризации акрилонитрила с бутадиеном (нитрильный каучук).
Поскольку полиакрилонитрил не растворялся в известных органических растворителях, его невозможно было перерабатывать в волокна. Впервые волокно из полиакрилонитрила получили с использованием в качестве растворителя диметилформамида.
Позднее было установлено, что полиакрилонитрил растворяется в концентрированном водном растворе роданида натрия или кальция. Это имело большое значение для усовершенствования технологии получения полиакрилонитрила.
Полиакрилонитрил и сополимеры на его основе нашли широкое применение в производстве волокон широкого назначения, бутадиен-нитрильного каучука, ударопрочного полистирола и других продуктов (1, С. 132).
1. Структура полиакрилонитрила
Полиакрилонитрил – труднокристаллизующийся линейный, карбоцепный полимер белого цвета. Структурная формула:
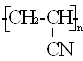
Методом ЯМР удалось установить, что микроструктура полиакрилонитрила зависит от условий полимеризации акрилонитрила. В присутствии радикальных инициаторов (например, перекиси бензоила, окислительно-восстановительных систем) при 40–80°С, а также анионных катализаторов (бутиллития) или под действием ![]() -излучения при -78°С образуется полиакрилонитрил одновременно синдио- и изотактической структуры (1:1). При получении полиакрилонитрила в канальных комплексах (например, в комплексе акрилонитрила с мочевиной) при -78°С и радиационном инициировании доля изотактической структуры возрастает до 75–90%.
-излучения при -78°С образуется полиакрилонитрил одновременно синдио- и изотактической структуры (1:1). При получении полиакрилонитрила в канальных комплексах (например, в комплексе акрилонитрила с мочевиной) при -78°С и радиационном инициировании доля изотактической структуры возрастает до 75–90%.
В зависимости от условий полимеризации акрилонитрила могут быть получены полимеры различного молекулярного веса (20000–350000).
Зависимость между молекулярной массой и характеристической вязкостью (![]() ), определяемой в диметилформамиде (С=2–20 г./л) при 20°С, выражается уравнением (
), определяемой в диметилформамиде (С=2–20 г./л) при 20°С, выражается уравнением (![]() )=K*10-3*M
)=K*10-3*M![]() , в котором Ки
, в котором Ки ![]() соответственно попарно равны: 1,75 и 0,66; 2,5 и 0,66; 0,233 и 0,75; 0,166 и 0,81; 0,392 и 0,75; 0,34 и 0,73; 0,317 и 0,746; 0,278 и 0,76. величины этих коэффициентов зависят от способа приготовления раствора акрилонитрила (3, С. 354).
соответственно попарно равны: 1,75 и 0,66; 2,5 и 0,66; 0,233 и 0,75; 0,166 и 0,81; 0,392 и 0,75; 0,34 и 0,73; 0,317 и 0,746; 0,278 и 0,76. величины этих коэффициентов зависят от способа приготовления раствора акрилонитрила (3, С. 354).
Молекулярно-массовое распределение полиакрилонитрила, соответствующее преобладающему способу обрыва цепи (рекомбинацией), характеризуется кривой с одним максимумом в случае гомогенной полимеризации (при отсутствии модифицирующего действия среды, например, диметилформамида или роданидов) и кривой с тремя максимумами в случае гетерофазной полимеризации. Специальные виды волокон (прочные, термостойкие) формуют из полиакрилонитрила, характеризующегося узким молекулярно-массовым распределением, т. к. максимально возможная при вытяжке ориентация уменьшается с увеличением полидисперсности. Полиакрилонитрил с наиболее узким молекулярно-массовым распределением образуется при анионной полимеризации акрилонитрила. При радикальной полимеризации акрилонитрила в гетерогенных условиях образуется полиакрилонитрил с наиболее широким молекулярно-массовым распределением.
Значение стерического фактора (гибкости) макромолекулы полиакрилонитрила ![]() =2,5–3,2, а длина сегмента Куна 3,17 нм (5, С. 150).
=2,5–3,2, а длина сегмента Куна 3,17 нм (5, С. 150).
2.1 Химические
Полиакрилонитрил при нагревании изменяет свой цвет, причем этот процесс всегда сопровождается потерей растворимости. Предполагается, что изменение окраски связано с образованием азометиновых мостиков между соседними макромолекулами, чему благоприятствует сильное притяжение, существующее между атомом азота и подвижным атомом водорода, находящимся в ![]() – положении:
– положении:
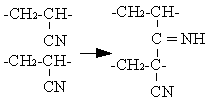
Стабилизация полиакрилонитрила и его сополимеров может быть произведена добавлением N-алкилоксиацетамидов (N, N-диметил-, N-этил-, N-метил-, N, N-диэтилоксиацетамидов). При стабилизации вводят 1–20% одного из указанных соединений. Для создания тепло- и светоустойчивых композиции можно приготовить при использовании стабилизаторов общей формулы R2NCH2СH2CN, например ![]() -диметиламинопропионитрила или
-диметиламинопропионитрила или ![]() -n-бутиламинопропионитрила (3, C. 354).
-n-бутиламинопропионитрила (3, C. 354).
Термическое воздействие (выше 150°С) вызывает необратимые изменения в химическом строении макромолекулы полиакрилонитрила, являющиеся результатом последовательного взаимодействия групп – CN между собой с образованием циклических структур. Это свойство полиакрилонитрила используется при изготовлении углеродных волокон (волокон специального назначения).
Производство углеродных волокон на основе ПАН волокон включает две стадии – термостабилизацию и карбонизацию. На стадии термостабилизации ПАН волокна нагревают приблизительно до 180–300°С в кислородсодержащей среде, при этом в структуре полимера протекает дополнительная ориентация. Образующиеся одновременно поперечные межмолекулярные связи между цепями позволяют избежать пиролиза при более высокой температуре. Довольно сложный химизм процесса стабилизации в основном включает в себя циклизацию нитрильных групп (C=N) и образование поперечных (межмолекулярных) связей цепных молекул, сопровождающееся дегидрированием и окислительными реакциями. В ходе этого процесса линейный полимер приобретает лестничную структуру (4, С. 30).
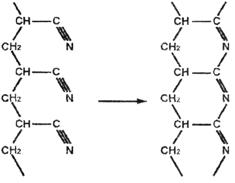
Образование хромофорных сопряженных связей – C=N–, вызывающее интенсивное окрашивание полиакрилонитрила в оранжево-коричневый и далее в черный цвет, промотируется нуклеофильными реагентами; наиболее эффективны карбоновые кислоты, фенолы, имиды и менее активны амиды, алифатические амины, спирты, альдегиды и кетоны (кроме ацетона). В инертной атмосфере такое превращение протекает гладко и вплоть до 220°С не приводит к разрушению основной полимерной цепи.
Нагревание на воздухе приводит к окислительному дегидрированию с образованием конденсированных нафтиридиновых структур и осложняется параллельно протекающими процессами термоокислительной деструкции полиакрилонитрила.

Продукты термического превращения полиакрилонитрила нерастворимы в обычных для полиакрилонитрила растворителях и обладают исключительно высокой термостойкостью: внесенные в пламя горелки порошок или волокно черного цвета из термообработанного полиакрилонитрила накаляются докрасна, но не горят (6, С. 44).
Полиакрилонитрил омыляется H2SO4конц. (75–95%-ная) на холоду; образуется хлопьевидный продукт белого цвета с молекулярной массой 62% от исходной, содержащий амидные (молярная концентрация до 90%) и имидные звенья:
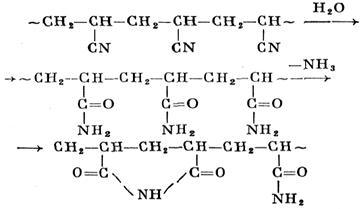
Этот продукт растворим в воде и слабых растворах кислот и щелочей, но не растворим в диметилформамиде. Пленки, полученные из 20%-ного водного раствора этого продукта, прозрачны и эластичны, но при высушивании становятся хрупкими; при 200°С они сильно темнеют и при 250–260°С разрушаются, не плавясь.
Нагревание полиакрилонитрила в процессе растворения в H2SO4 приводит к полному исчезновению амидных и имидных групп и образованию карбоксильных групп.
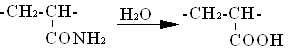
При обработке полиакриламида раствором соды степень омыления достигает 30–40%. По деструктивному действию омыляющие агенты можно расположить в следующий возрастающий ряд: NaOH (1%-ный), НС1, НСООН, Na2CO3, H2SO4, H3PO4. При взаимодействии полиакрилонитрила с гидроксиламином при 50–100°С протекает реакция образования амидоксимных групп с последующим выделением аммиака и образованием групп гидроксамовой кислоты:

Для реакции применяется раствор сернокислого гидроксиламина и едкого натра в количестве, достаточном для выделения – 99,2% гидроксиламина. Полимер после реакции содержит как группы гидроксамовой кислоты, так и непрореагировавшие нитрильные группы. Наличие в полимере групп гидроксамовой кислоты способствует лучшему окрашиванию полиакрилонитрильного волокна.
Полиакрилонитрил в отличие от других акриловых смол не растворяется в обычных растворителях. Эта особенность объясняется значительными межмолекулярными силами, возникающими вследствие полярной природы – С = N-групп. Представления о влиянии водородных связей в полимерах на их растворимость в полярных растворителях и установление растворимости полиакрилонитрила в гидротропных растворителях (например, в концентрированном водном растворе роданистого кальция), послужили толчком к поискам высокополярных растворителей.
Так как группа – CN является сильно полярной, то полиакрилонитрил растворяется только в очень полярных растворителях, например, в диметилформамиде, диметилацетамиде, этиленкарбонате, диметилсульфоксиде, концентрированных водных растворах бромистого лития, роданистого натрия или кальция, смеси ZnCl2+CaCl2, концентрированных HNO3 и H2SO4 (в последнем случае группы – CN гидролизуются).
Показатель растворимости полиакрилонитрила ![]() =30,8*10-3 (Дж/м3)0,5, а воды
=30,8*10-3 (Дж/м3)0,5, а воды ![]() =46,4*10-3 (Дж/м3)0,5 напомним, что растворение полимера в растворителе происходит при значениях
=46,4*10-3 (Дж/м3)0,5 напомним, что растворение полимера в растворителе происходит при значениях ![]() 4 (Дж/м3)0,5, т.е.
4 (Дж/м3)0,5, т.е. ![]() должен быть почти равен
должен быть почти равен ![]() , что для воды и полиакрилонитрила не наблюдается (4, C. 99).
, что для воды и полиакрилонитрила не наблюдается (4, C. 99).
При нагревании полиакрилонитрил растворяется в N-формилпиперидине (170–180°С), цианацетамиде (165–170°С), N-метил-иианацетамиде (180–190°С), этиленциангидрине (165–170°С), однако при охлаждении этих растворов образуются гели (происходит застудневание). Предполагается, что механизм застудневания растворов полиакрилонитрила заключается в образовании трехмерной сетки за счет возникновения вторичных межмолекулярных связей. Скорость застудневания повышается при увеличении концентрации растворов, молекулярного веса полимера и количества введенной воды (6, С. 43).
Растворители способные разрушить межмолекулярные связи в полимере это диметилформамид и тетраметиленсульфон, динитрил малоновой и янтарной кислот, смеси, содержащие более 60% этиленкарбоната и воды, диметилцианамид, концентрированные водные растворы некоторых солей, например бромистого лития, роданистого натрия и кальция, хлористого цинка.
Для снижения растворимости полиакрилонитрил обрабатывают водным раствором формальдегида.
Таблица 1 Свойства полиакрилонитрила
| Свойство | Значение |
Плотность, г/см3 | 1,14–1,15 |
Показатель преломления, n | 1,49–1,52 |
| Температура размягчения (с одновременной деструкцией), °С | 220–230 |
| Удельная теплоемкость, кДж/(кг*К) (кал/(г*°С)) | 1,51 |
Прочность при растяжении (для волокна), Мн/м2 (кгс/мм2) | 600 (60) |
| Относительное удлинение, % | 10–35 |
| Влагопоглощение отпрессованного образца, % | 1–2 |
| Дипольный момент, к*м (D) | 1,13–10-4 |
| Диэлектрическая проницаемость при | |
| 50 гц | 6,5 |
| 1 Мгц | 4,2 |
| Удельное объемное электрическое сопротивление, Том*м (Ом*см) | 1 (1014) |
| Тангенс угла диэлектрических потерь при | |
| 50 гц | 0,11 |
1Мгц | 0,03 |
Подобные работы: