Механизмы дыхания растений
1.Дыхание. Определение. Уравнение. Значение дыхания в жизни растительного организма. Специфика дыхания у растений
Образующиеся в ходе фотосинтеза сахара и другие органические соединения используются клетками растительного организма в качестве питательных веществ. Клетки незеленых частей и все клетки растения в темноте питаются веществами углеводной природы гетеротрофно и в этом принципиально не отличаются от животных клеток. Важнейшим этапом питания органическими веществами на клеточном уровне является процесс дыхания.
Клеточное дыхание — это окислительный, с участием кислорода распад органических питательных веществ, сопровождающийся образованием химически активных метаболитов и освобождением энергии, которые используются клетками для процессов жизнедеятельности.
Научные основы учения о роли кислорода в дыхании были заложены трудами A. Л. Лавуазье. В 1774 г. кислород независимо открыли Пристли и Шееле, а Лавуазье дал название этому элементу. Изучая одновременно процесс дыхания животных и горение, Лавуазье в 1773 — 1783 гг. пришел к выводу. что при дыхании, как и при горении, поглощается 02 и образуется С02, причем в том и другом случаях выделяется теплота. На основании своих опытов он заключил, что процесс горения состоит в присоединении кислорода к субстрату и что дыхание есть медленно текущее горение питательных веществ в живом организме.
Я. Ингенхауз в 1778—1780 гг. показал, что зеленые растения в темноте, а незеленые части растений и в темноте, и на свету поглощают кислород и выделяют С02 так же, как животные. Основателем учения о дыхании растений считают Н. Т. Соссюра. В 1797—1804 гг., впервые широко использовав количественный анализ, он установил, что в темноте растения поглощают столько же кислорода, сколько выделяется С02, т.е. соотношение С02/02, как правило, равно 1. При этом одновременно с С02 образуется и вода. Мнение Соссюра о том. что описанный им газообмен у растений является процессом дыхания и что этот процесс обеспечивает растительный организм энергией, долгое время не признавалось. Утверждалось, что в ночное время растения выделяют тот С02, который не был использован при фотосинтезе, и что этот С02 не имеет отношения к дыханию.
Однако постепенно накапливалось все больше данных о том, что дыхание животных и растений протекает однотипно, несмотря на отсутствие у растений специальных дыхательных органов, причем основным субстратом дыхания служат сахара. И. П. Бородин (1876) в серии точных опытов установил, что интенсивность дыхания листоносных побегов в темноте в первую очередь зависит от количества углеводов, накопленных ими на свету.
Во второй половине XIX в. в результате изучения дыхания у растительных и животных объектов общее уравнение этого процесса приняло следующий вид:
С6Н12О6 + 602 ► 6С02 + 6Н20 + энергия (2875 кДж/моль)
ЗНАЧЕНИЕ ДЫХАНИЯ В ЖИЗНИ РАСТЕНИЯ
Дыхание — один из центральных процессов обмена веществ растительного организма. Выделяющаяся при дыхании энергия тратится как на процессы роста, так и нa поддержание в активном состоянии уже закончивших рост органов растения. Вместе с тем значение дыхания не ограничивается тем, что это процесс, поставляющий энергию. Дыхание, подобно фотосинтезу, сложный окислительно_восстановительный процесc, идущий через ряд этапов. На его промежуточных стадиях образуются органические соединения, которые затем используются в различных метаболических реакциях. К промежуточным соединениям относят органические кислоты и пентозы образующиеся при разных путях дыхательного распада. Таким образом, процесс дыхания — источник многих метаболитов. Несмотря на то что процесс дыхания в суммарном виде противоположен фотосинтезу, в некоторых случаях они могут дополнять друг друга. Оба процесса являются поставщиками как энергетических эквивалентов (АТФ, НАДФ-Н), так и метаболитов. Как видно из суммарного уравнения, в процессе дыхания образуется также вода. Эта вода в крайних условиях обезвоживания может быть использована растением и предохранить его от гибели. В некоторых случаях, когда энергия дыхания выделяется в виде тепла, дыхание ведет к бесполезной потере сухого вещества. В этой связи при рассмотрении процесса дыхания надо помнить, что не всегда усиление процесса дыхания является полезным для растительного организма.
2.Основные этапы становления учения о дыхании растений
Если, по Лавуазье, дыхание имеет сходство с процессом горения, то каким же образом органические вещества могут «гореть» при обычной температуре тела организма, да еще в водной среде, (ведь на 70 — 90% масса живых организмов состоит из воды)? Возникло предположение о том, что в живых клетках существуют механизмы, активирующие кислород. Швейцарский химик X. Ф. Шейнбайн, открывший озон, изучал причины быстрого потемнения пораненной поверхности растительных тканей, таких, как ткани яблок, картофеля, плодовых тел грибов. В 1845 г. он выступил со своей теорией окислительных процессов, согласно которой в живых клетках имеются соединения, способные легко окисляться в присутствии 02 и таким образом активировать молекулярный кислород. Если ткань прокипятить, то потемнения не происходит. Следовательно, потемнение тканей — каталитический окислительный процесс. Шейнбайн ошибочно полагал, что активация кислорода — это образование озона.
Исследования, начатые Шейнбайном, продолжил А. Н. Бах, который в 1897 г. разработал перекисную теорию биологического окисления, приложив ее к процессам дыхания. Несколько позже, в том же 1897 г., аналогичные взгляды высказал немецкий исследователь К. Энглер.
Суть перекисной теории биологического окисления Баха заключается в следующем. Молекулярный кислород имеет двойную связь и для того чтобы его активировать, необходимо эту двойную связь расщепить. Легко окисляющееся соединение А взаимодействует с кислородом и, разрывая двойную связь, образует пероксид А02 Таким образом, по мысли Баха, активация кислорода есть образование пероксида. В свою очередь пероксидное соединение, взаимодействуя с соединением В, окисляет его; затем эта реакция повторяется со вторым атомом кислорода и второй молекулой соединения В. Получается полностью восстановленное исходное соединение — акцептор кислорода А и полностью окисленное вещество В:
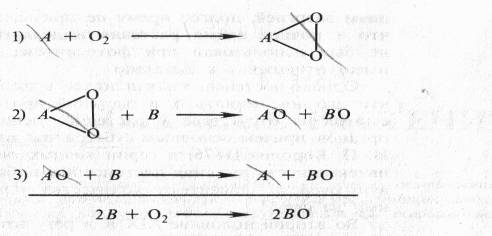
Во второй и третьей реакциях, по Баху, участвует пероксидаза. Соединение А, которое активирует кислород, Бах назвал «оксигеназой», рассматривая его вначале как фермент. В дальнейшем он пришел к заключению, что это те соединения, которые темнеют на воздухе при поранении тканей, что именно такого рода легко окисляющиеся вещества способны присоединять кислород и образовывать пероксиды.
Много позднее, в 1955 г., две группы исследователей — О. Хаяиши с сотр. в Японии и Г. С. Мэзон с сотр. в США, используя современные методы, проанализировали возможность включения кислорода в органические соединения. Применив тяжелый изотоп кислорода, Хаяиши изучил процесс окисления пирокатехина до пирокатеховой кислоты под действием пирокатехазы:
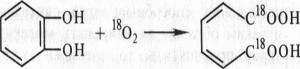
Кислород в пирокатеховой кислоте оказался меченым. Таким образом, в точном эксперименте было доказано, что молекулярный кислород действительно может включаться в органические соединения.
В настоящее время известно, что путь включения кислорода в органические соединения в соответствии с перекисной теорией биологического окисления Баха и Энглера не имеет отношения к дыханию, однако работы этих исследователей сыграли большую роль в изучении химизма дыхания, заложив основы современного понимания механизмов активации кислорода.
Какую же роль играет кислород в процессах дыхания? В 1921 г. немецкий биохимик О. Г. Варбург, изучая влияние ингибиторов на дыхание различных объектов, обнаружил, что поглощение кислорода резко ингибируется оксидом углерода и синильной кислотой, взаимодействующими в клетках с железосодержащим веществом порфириновой природы (с цитохромоксидазой). Английский биохимик Д. Кейлин в 1925 г. окончательно доказал присутствие в клетках цитохромоксидазы, ускоряющей поглощение ими кислорода, и открыл другие цитохромы. Затем цитохромы были обнаружены у всех аэробов и было показано, что у этих организмов на завершающем этапе процесса дыхания осуществляется перенос на кислород электронов и протонов, в результате чего образуется Н20 (или Н202).
Органические соединения могут окисляться и другим способом благодаря отнятию водорода. Еще Бах, сделав упор на перекисную теорию, выдвинул и вторую гипотезу, согласно которой биологическое окисление связано с отнятием от субстрата электронов и протонов. Роль же кислорода состоит в этом случае в регенерации окисленного состояния первичного акцептора водорода. По Баху, последовательность реакций в процессе могла бы выглядеть следующим образом:
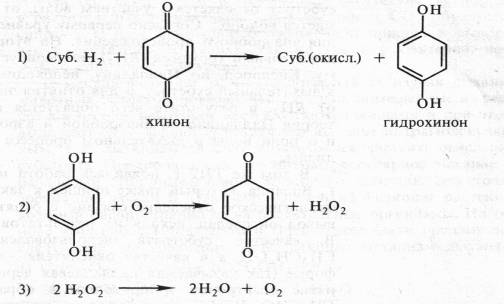
Эта вторая гипотеза Баха в дальнейшем была развита В. И. Палладиным в стройную теорию химизма дыхания. Занимаясь с 1903 по 1916 г. дыхательными пигментами (темнеющими на воздухе веществами тканей), Палладин нашел удачную искусственную модель, которая помогла расшифровать химизм дыхания. Это был известный краситель метиленовый синий. Если в пробирку с раствором метиленового синего поместить несколько прорастающих зародышей пшеницы и выкачать воздух (удалить кислород), то через некоторое время этот краситель полностью обесцветится. Если затем открыть пробирку и встряхнуть содержимое (т. е. дать кислород), то краситель снова синеет. Таким образом, при контакте с кислородом краситель окисляется, приобретая синий цвет, а живая ткань способна восстанавливать краситель, обёсцве чивая его. Причем окисление метиленового синего связано не с присоединением кислорода, а с отнятием водорода. Краситель восстанавливается за счет присоединения электронов и протонов.
На основании этих и других опытов Палладин в 1912 г. в статье «Значение дыхательных пигментов в окислительных процессах растений и животных» представил общую теорию химизма дыхания, разделив основное уравнение дыхания на анаэробную (1) и аэробную (2) части:

гдеR — это окрашенный дыхательный пигмент, способный отнимать водород от субстрата, a RH2 — бесцветный дыхательный хромоген. На первом, анаэробном, этапе дыхания глюкоза окисляется за счет отнятия водорода, который с помощью фермента (редуктазы) передается на дыхательный пигментR (активация водорода!). По Палладину, дыхательный субстрат окисляется с участием воды, от которой тоже отнимается водород. Согласно первому уравнению весь С02 дыхания анаэробного происхождения. На втором, аэробном, этапе дыхательный хромоген (RН2) регенерирует в окисленную форму. Кислород, по Палладину, необходим не для включения в дыхательный субстрат, а для отнятия электронов и протонов от RН2, в результате чего образуется вода. В дальнейшем теория Палладина об анаэробной и аэробной фазах дыхания и о роли воды в дыхательном процессе полностью подтвердилась.
В том же 1912 г. появилась работа немецкого биохимика Г. Виланда, который также пришел к заключению о том, что биологическое окисление связано с отнятием водорода. Этот вывод он сделал, исходя из результатов модельных опытов. В качестве субстрата использовался этиловый спирт СН3СН2ОН, а в качестве окислителя — палладий в губчатой форме (так называемая палладиевая чернь). Происходило отнятие электронов и протонов и образовывался альдегид СН3СНО. Чтобы регенерировать восстановленный палладий и сделать реакцию долгоидущей, Виланд вводил хинон:
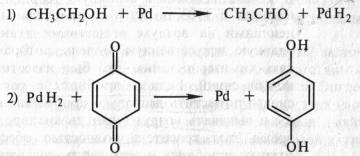
Эта реакция проводилась в небиологической системе и не предусматривала участие кислорода и воды.
Экспериментальные доказательства участия воды в окислении субстрата дыхания и роли 02 как конечного акцептора водорода были получены лишь в 1955 г. в работе Б. Б. Вартапетяна и A. Л. Курсанова. Опыты ставились с этиолированными проростками пшеницы, которым давали 180 в составе 02 или Н20, а через 2 ч анализировали содержание 180 в С02 дыхания
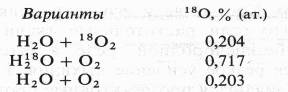
В состав С02 при дыхании тяжелый изотоп кислорода входил из меченой воды, но не из молекулярного кислорода.
Из всех приведенных выше данных следует, что окисление органических веществ в ходе дыхания связано с отнятием водорода и что теория Лавуазье о сходстве дыхания и горения не соответствует действительности.
3.Каталитические системы дыхания
Окисление дыхательных субстратов в ходе дыхания осуществляется с участием ферментов. Ферменты как белковые катализаторы, помимо свойств, присущих неорганическим катализаторам, обладают рядом особенностей: высокой актианостью, высокой специфичностью по отношению к субстратам и высокой лабильностью. Их пространственная организации зависящая от нее активность изменяются под действием внешних и внутренних факторов. Эти свойства обеспечивают возможность тонкой регуляции обмена веществ на уровне ферментов.
Типы окислительно-восстановительных реакций. Существуют четыре способа окисления, и все они связаны с отнятием электронов:
1) непосредственная отдача электронов, например:
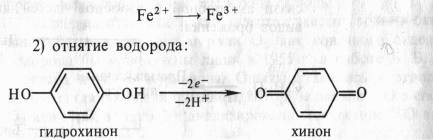
3) присоединение кислорода
![]()
4) образование промежуточного гидратированного соединения с последующим отнятием двух электронов и протонов:
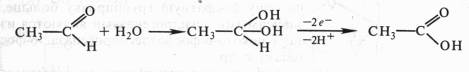
Оксидоредуктазы.
Поскольку окисление одного вещества (донора электронов и протонов) сопряжено с восстановлением другого соединения (их акцептора), ферменты, катализирующие эти реакции, называют оксидоредуктазами. Все они относятся к I классу ферментов:
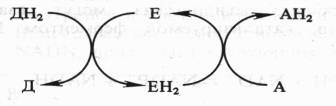
Донор (Д) отдает электроны и протоны, акцептор (А) принимает их, а энзим (Е) осуществляет реакцию переноса. Существуют три группы оксидоредуктаз:
а) анаэробные дегидрогеназы передают электроны различным промежуточным акцепторам, но не кислороду;
б) аэробные дегидрогеназы передают электроны различным акцепторам, в том числе кислороду;
в) оксидазы способны передавать электроны только кислороду.
Анаэробные дегидрогеназы. Это двухкомпонентные ферменты, коферментом которых может быть NAD+ (никотинамидадениндинуклеотид):
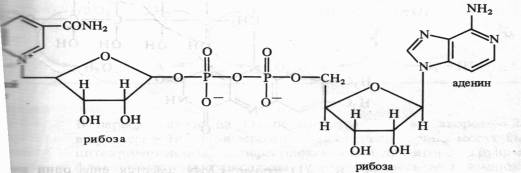
При окислении субстрата NAD+ превращается в восстановленную форму NADH, а второй протон субстрата диссоциирует в среду (NADH + Н + ). К анаэробным NAD-зависимым дегидрогеназам относятся такие ферменты, как алкогольдегидрогеназа, лактатдегидрогеназа, малатдегидрогеназа и др. Коферментом анаэробных дегидрогеназ может быть также NADP+ (никотинамидадениндинуклеотидфосфат), содержащий на одну фосфатную группировку больше, чем NAD + . NADP- зависимыми дегидрогеназами являются изоцитратдегидрогеназа, глюкозо-6-фосфатдегидрогеназа, 6-фосфоглюконатдегидрогеназа и др.
Субстратная специфичность фермента зависит от его белковой части. Многие NAD- и NADP-зависимые дегидрогеназы нуждаются в присутствии ионов двухвалентных металлов. Например, алкогольдегидрогеназа содержит ионы цинка.
Окисленные и восстановленные формы коферментов анаэробных дегидрогеназ могут взаимопревращаться в реакции, катализируемой ферментом NAD(Р)-трансгидрогеназой:
NADPH + NAD+ = NADP+ + NADH
Анаэробные дегидрогеназы передают водород, т. е. электроны и протоны, различным промежуточным переносчикам и аэробным дегидрогеназам.
Аэробные дегидрогеназы. Это также двухкомнонентные ферменты, получившие название флавиновых (флавопротеины).
Помимо белков, в их состав входит прочно связанная с ними простетическая группа — рибофлавин (витамин В2).
Различают два кофермента этой группы: флавинмононуклеотид (FMN), или желтый дыхательный фермент Варбурга, и флавинадениндинуклеотид (FAD).
FMN (рибофлавин-5-фосфат) содержит гетероциклическое азотистое основание — диметилизоаллоксазин, спирт рибит (производное рибозы) и фосфат:
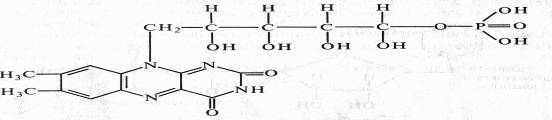
В FAD кроме FMN имеется еще один нуклеотид — аденозинмонофосфата:
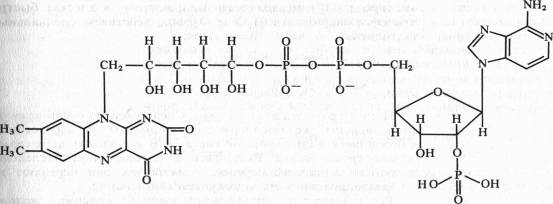
Активной группой в реакции присоединения и отдачи электронов и протонов в FMN и FAD служит изоаллоксазин. Взаимодействие с восстановленным переносчиком, например NADH, происходит следующим образом:
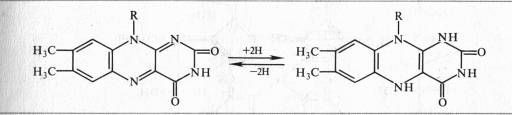
Примером дегидрогеназы, в состав которой входит FAD, является сукцинатдегидрогеназа. Доноры электронов для аэробных дегидрогеназ — анаэробные дегидрогеназы, а акцепторы — хиноны, цитохромы, кислород.
Цитохромная система. Среди оксидаз очень важную роль играют железосодержащие ферменты и переносчики, относящиеся к цитохромной системе. В нее входят цитохромы " и цитохромоксидаза. Включаясь в определенной последовательности в процесс переноса электронов, они передают их от флавопротеинов на молекулярный кислород.
Все компоненты цитохромной системы содержат железопорфириновую простетическую группу.
При переносе электронов цитохромами железо обратимо окисляется и восстанавливается, отдавая или приобретая электрон и изменяя таким образом свою валентность. В дыхательной цепи направление транспорта электронов определяется величиной окислительно-восстановительного потенциала цитохромов.
В этой системе передавать электроны непосредственно на кислород способна только цитохромоксидаза (цит. а + а3). Из всех известных оксидаз она имеет наибольшее сродство к кислороду. Ингибиторами цитохромоксидазы являются СО, цианид, азид. Б растительных митохондриях кроме цитохромоксидазы функционирует оксидаза, не подавляемая цианидом и названная альтернативной оксидазой. Например, в митохондриях початков ароидных активность цианидустойчивой оксидазы в 10 раз превышает активность цитохромоксидазы.
Пероксидаза и каталаза. К пероксидазам относят целую группу ферментов, использующих в качестве окислителя пероксид водорода: классическую пероксидазу, NAD-пероксидазу, NADP-пероксидазу, пероксидазу жирных кислот, глутатионпероксидазу, цитохромпероксидазу и др. Все они работают по следующей схеме, где А — субстраты:
![]()
В последние 2 — 3 десятилетия показана полифункциональность пероксидаз. Помимо пероксидазной, у них имеется оксидазная функция, т. е. способность переносить электроны в отсутствие пероксидного кислорода на молекулярный кислород. Пероксидаза может также функционировать как анаэробная дегидрогеназа, например NADH-дегидрогеназа, передающая электроны от восстановленных пиридиновых нуклеотидов на разные акцепторы.
Пероксид водорода, помимо пероксидазы, расщепляется также каталазой, в результате чего образуется молекулярный кислород. В реакции участвуют две молекулы пероксида, одна из которых функционирует как донор, а другая — как акцептор электронов (см. выше).
Простетической группой пероксидазы и каталазы служит гем, в состав которого входит атом железа.
Оксигеназы. Наряду с оксидазами, которые используют молекулярный кислород как акцептор электронов, в клетках широко представлены оксигеназы, активирующие кислород, в результате чего он может присоединяться к органическим соединениям. Ферменты, внедряющие в субстрат два атома кислорода, называют диоксигеназами, а присоединяющие один атом кислорода — монооксигеназами или гидроксилазами. В качестве доноров электронов оксигеназы используют NAD(P)H, FADH2 и др.
Оксигеназы присутствуют во всех типах клеток. Они участвуют в гидроксилировании многих эндогенных соединений в частности аминокислот, фенолов, стеринов и др., а также в детоксикации чужеродных токсических веществ (ксенобиотиков).
4.Основные пути диссимиляции углерода
Существуют три основных пути диссимиляции углерода. Основной дихотомический путь который включает в себя гликолиз и цикл Кребса. Есть также апотонический путь который включает в себя пентозофосфатный цикл. Путем диссимиляции запасных веществ служит глиоксилатный цикл.
4.1 Дихотомический путь
4.1.1Гликолиз. Механизмы регуляции цикла. Энергетическая эффективность процесса, значение. Связь с другими процессами
Гликолиз — процесс анаэробного распада глюкозы, идущий Гликолиз с освобождением энергии, конечным продуктом которого является пировиноградная кислота. Гликолиз — общий начальный этап аэробного дыхания и всех видов брожения. Реакции гликолиза протекают в растворимой части цитоплазмы (цитозоле) и в хлоропластах. В цитозоле гликолитические ферменты, по-видимому, организованы в мультиэнзимные комплексы с участием актиновых филаментов цитоскелета, с которыми гликолитические ферменты обратимо связываются с разной степенью прочности. Такое связывание обеспечивает векторность процесса гликолиза.
Английский биохимик А. Гарден и ученик К. А. Тимирязева Л. А. Иванов в 1905 г. независимо показали, что в процессе спиртового брожения наблюдается связывание неорганического фосфата и превращение его в органическую форму. Гарден установил, что глюкоза подвергается анаэробному распаду только после ее фосфорилирования. Полностью весь процесс гликолиза расшифровали немецкие биохимики Г. Эмбден, О. Ф. Мейергоф и советский биохимик Я. О. Парнас, с именами которых связывают название этого катаболического
Цепь реакций, составляющих суть гликолиза, можно разбить на три этапа (рис. 4.1):
I. Подготовительный этап — фосфорилирование гексозы и ее расщепление на две фосфотриозы.
II. Первое субстратное фосфорилирование, которое начинается с 3-фосфоглицеринового альдегида и кончается 3-фосфоглицериновой кислотой. Окисление альдегида до кислоты связано с освобождением энергии. В этом процессе на каждую фосфотриозу синтезируется одна молекула АТР.
III. Второе субстратное фосфорилирование, при котором 3-фосфоглицериновая кислота за счет внутримолекулярного окисления отдает фосфат с образованием АТР.
Поскольку глюкоза стабильное соединение, на ее активацию необходима затрата энергии, что осуществляется в процессе образования фосфорных эфиров глюкозы в ряде подготовительных реакций. Глюкоза (в пиранозной форме) фосфорилируется АТР с участием гексокиназы, превращаясь в глюкозо-6-фосфат, который изомеризуется в фруктозо-6-фосфат с помощью глюкозофосфатизомеразы. Этот - переход необходим для образования более лабильной фуранозной формы молекулы гексозы. Фруктозо-6-фосфат фосфорилируется вторично фосфофрукгокиназой с использованием еще одной молекулы АТР.
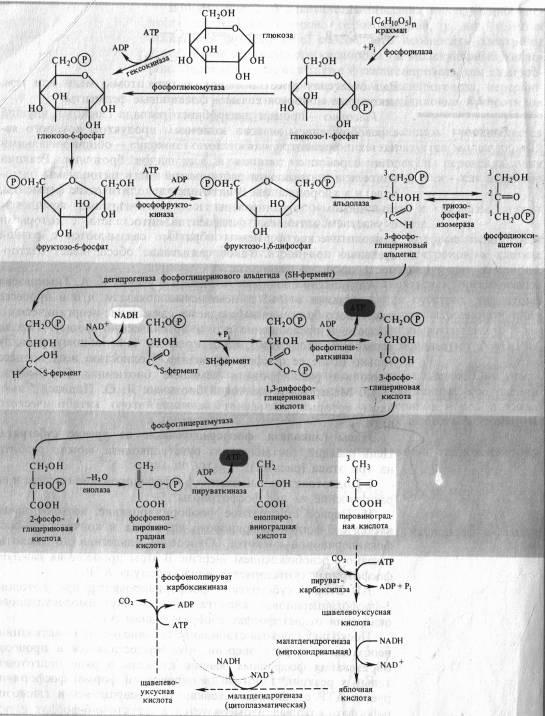
Фруктозо-1,6-дифосфат — лабильная фуранозная форма с симметрично расположенными фосфатными группами. Обе эти группы несут отрицательный заряд, отталкиваясь друг от друга электростатически. Такая структура легко расщепляется аль- долазой на две фосфотриозы. Следовательно, смысл подготовительного этапа состоит в активации молекулы гексозы за счет двойного фосфорилирования и перевода в фуранозную форму с последующим распадом на 3-фосфоглицериновый альдегид (3-ФГА) и фосфодиоксиацетон (ФДА), причем бывший 6-й атом углерода в молекуле глюкозы и фруктозы (фосфорилированный) становится 3-м в 3-ФГК, а 1-й атом углерода фруктозо-1,6-дифосфата остается 1-м углеродом (фосфорилированным) в ФДА (см. рис. 4.1). 3-ФГА и ФДА легко превращаются друг в друга с участием триозофосфатизомеразы. Из-за расщепления молекулы гексозы на две триозы гликолиз иногда называют дихотомическим путем окисления глюкозы.
С 3-ФГА начинается II этап гликолиза — первое субстратное фосфорилирование. Фермент дегидрогеназа фосфоглицеринового альдегида (NAD-зависимый SH-фермент) образует с 3-ФГА фермент-субстратный комплекс, в котором происходит окисление субстрата и передача электронов и протонов на NAD + . В ходе окисления фосфоглицеринового альдегида до фосфоглицериновой кислоты в фермент-субстратном комплексе возникает меркаптанная высокоэнергетическая связь (т. е. связь с очень высокой свободной энергией гидролиза). Далее осуществляется фосфоролиз этой связи, в результате чего SH-фермент отщепляется от субстрата, а к остатку карбоксильной группы субстрата присоединяется неорганический фосфат, причем ацилфосфатная связь сохраняет значительный запас энергии, освободившейся в результате окисления 3-ФГА. Высокоэнергетическая фосфатная группа с помощью фосфоглицераткиназы передается на ADP и образуется АТР. Так как в данном случае высокоэнергетическая ковалентная связь фосфата формируется прямо на окисляемом субстрате, такой процесс получил название субстратного фосфорилирования. Таким образом, в результате II этапа гликолиза образуются АТР и восстановленный NADH.
Последний этап гликолиза — второе субстратное фосфорилирование. З-Фосфоглицериновая кислота с помощью фосфоглицератмутазы превращается в 2-фосфоглицериновую кислоту. Далее фермент енолаза катализирует отщепление молекулы воды от 2-фосфоглицериновой кислоты. Эта реакция сопровождается перераспределением энергии в молекуле, в результате чего образуется фосфоенолпируват — соединение, содержащее высокоэнергетическую фосфатную связь. Таким образом, в этом случае высокоэнергетическая фосфатная связь формируется на основе того фосфата, который имелся в самом субстрате. Этот фосфат при участии пируваткиназы передается на ADP и образуется АТР, а енолпируват самопроизвольно переходит в более стабильную форму — пируват — конечный ппопукт гликолиза.
Энергетическийвыход гликолиза. При окислении одной молекулы глюкозы образуются две молекулы пировиноградной кислоты. При этом за счет первого и второго субстратного фосфорилирования образуются четыре молекулы АТР. Однако две молекулы АТР тратятся на фосфорилирование гексозы на I этапе гликолиза. Таким образом, чистый выход гликолитического субстратного фосфорилирования составляет две молекулы АТР.
Кроме того, на II этапе гликолиза на каждую из двух молекул фосфотриоз восстанавливается по одной молекуле NADH. Окисление одной молекулы NADH в электронтранспортной цепи митохондрий в присутствии 02 сопряжено с синтезом трех молекул АТР, а в расчете на две триозы (т. е. на одну молекулу глюкозы) - шесть молекул АТР. Таким образом, всего в процессе гликолиза (при условии последующего окисления NADН) образуются восемь молекул АТР. Поскольку свободная энергия гидролиза одной молекулы АТР во внутриклеточных условиях составляет около 41,868 кДж/моль (10 ккал), восемь молекул АТР дают 335 кДж/моль, или 80 ккал. Таков полный энергетический выход гликолиза в аэробных условиях.
Обращение гликолиза. Возможность обращения гликолиза определяется обратимостью действия большинства ферментов, катализирующих его реакции. Однако реакции фосфорилирования глюкозы и фруктозы, а также реакция образования пировиноградной кислоты из фосфоенолпирувата, осуществляемые с помощью киназ, необратимы. На этих участках процесс обращения идет благодаря использованию обходных путей. |Там, где функционируют гексокиназа и фруктокиназа, происходит дефосфорилирование — отщепление фосфатных групп фосфатазами.
Превращение пирувата в фосфоенолпируват также не может осуществиться путем прямого обращения пируваткиназной реакции вследствие большого перепада энергии. Первая реакция обращения гликолиза на этом участке катализируется митохондриальной пируваткарбоксилазой в присутствии АТР и ацетил-СоА (последний выполняет функции активатора).
(Образующаяся щавелевоуксусная кислота (ЩУК), или оксалоацетат, восстанавливается затем в митохондриях до малата при участии NAD-зависимой малатдегидрогеназы (МДГ). Затем малат транспортируется из митохондрий в цитоплазму, где окисляется NAD-зависимой цитоплазматической малатдегидрогеназой снова до ЩУК. Далее под действием ФЕП-карбоксикиназы из оксалоацетата образуется фосфоенолпируват. Фосфорилирование в этой реакции осуществляется за счет АТР (см. рис. 4.1).
Функции гликолиза в клетке. В аэробных условиях гликолиз выполняет ряд функций: 1) осуществляет связь между дыхательными субстратами и циклом Кребса; 2) поставляетнанужды клетки две молекулы АТР и две молекулы NADHпри окислении каждой молекулы глюкозы (в условиях аноксии гликолиз, по-видимому, служит основным источником АТР в клетке); 3) производит интермедиа, необходимые для синтетических процессов в клетке (например, фосфоенолпируват, необходимый для образования фенольных соединений и лигнина); 4) в хлоропластах гликолитические реакции обеспечивают прямой путь для синтеза АТР, независимый от поставок NADPH; кроме того, через гликолиз в хлоропластах запасенный крахмал метаболизируется в триозы, которые затем экспортируются из хлоропласта.
Регуляция гликолиза.
Интенсивность гликолиза контролируется в нескольких участках. Вовлечение глюкозы в процесс гликолиза регулируется на уровне Фермента гексокиназы по типу обратной связи: избыток продукта реакции (глюкозо-6-фосфата) аллостерически подавляет деятельность фермента.
Второй участок регуляции скорости гликолиза находится на уровне фосфофруктокиназы. Фермент аллостерически ингибируется высокой концентрацией АТР и активируется неорганическим фосфатом и ADP. Ингибирование АТР предотвращает развитие реакции в обратном направлении при высокой концентрации фруктозо-6-фосфата. Кроме того, фермент подавляется продуктом цикла Кребса — цитратом и через положительную обратную связь активируется собственным продуктом — фруктозо-1,6-дифосфатом (самоусиление).
Высокие концентрации АТР подавляют активность пируваткиназы, снижая сродство фермента к фосфоенолпирувату. Пируваткиназа подавляется также ацетил-СоА.
Наконец, пируВатдегидрогеназный комплекс, участвующий в образовании ацетил-СоА из пирувата, ингибируется высокими концентрациями АТР, а также NADH и собственным продуктом — ацетил-СоА.
4.1.2 Цикл Кребса. Механизмы регуляции цикла. Энергетическая эффективность процесса, значение
В анаэробных условиях пировиноградная кислота (пируват) подвергается дальнейшим превращениям в ходе спиртового, молочнокислого и других видов брожений, при этом NADH используется для восстановления конечных продуктов брожения, регенерируя в окисленную форму. Последнее обстоятельство поддерживает процесс гликолиза, для которого необходим окисленный NAD + . В присутствии достаточного количества кислорода пируват полностью окисляется до С02 и Н20 в дыхательном цикле, получившем название цикла Кребса или цикла ди- и трикарбоновых кислот. Все участки этого процесса локализованы в матриксе или во внутренней мембране митохондрий.
Последовательностьреакций в цикле Кребса. Участие органических кислот в дыхании давно привлекало внимание исследователей. Еще в 1910 г. шведский химик Т. Тунберг показал, что в животных тканях содержатся ферменты, способные отнимать водород от некоторых органических кислот (янтарной, яблочной, лимонной). В 1935 г. А. Сент-Дьердьи в Венгрии установил, что добавление к измельченной мышечной ткани небольших количеств янтарной, фумаровой, яблочной или щавелевоуксуснсй кислот резко активирует поглощение тканью кислорода.
Учитывая данные Тунберга и Сент-Дьердьи и исходя из собственных экспериментов по изучению взаимопревращения различных органических кислот и их влияния на дыхание летательной мышцы голубя, английский биохимик Г. А. Кребс в 1937 г. предложил схему последовательности окисления ди- и трикарбоновых кислот до С02 через «цикл лимонной кислоты» да счет отнятия водорода. Этот цикл и был назван его именем.
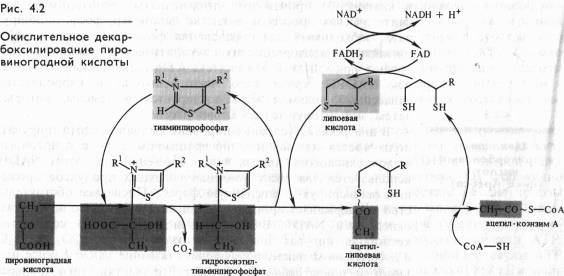
Непосредственно в цикле окисляется ле сам пируват, а его производное — ацетил-СоА. Таким образом, первым этапом на пути окислительного расщепления ПВК является процесс образования активного ацетила в ходе окислительного декарбоксилирования. Окислительное декарбоксилирование пирувата осуществляется при участии пируватдегидрогеназного мультифёрментного комплекса. В состав его входят три фермента и пять коферментов. Коферментами служат тиаминпирофосфат (ТПФ) — фосфорилированное производное витамина Вь липоевая кислота, коэнзим A, FAD и NAD+. Пируват взаимодействует с ТПФ (декарбоксилазой), при этом отщепляется С02 и образуется гидроксиэтильное производное ТПФ (рис. 4.2). Последнее вступает в реакцию с окисленной формой липоевой кислоты. Дисульфидная связь липоевой кислоты разрывается и происходит окислительно-восстановительная реакция: гидроксиэтильная группа, присоединенная к одному атому серы, окисляется в ацетильную (при этом возникает высокоэнергетическая тиоэфирная связь), а другой атом серы липоевой кислоты восстанавливается. Образовавшаяся ацетиллипоевая кислота взаимодействует с коэнзимом А, возникают ацетил- СоА и восстановленная форма липоевой кислоты. Водород липоевой кислоты переносится затем на FAD и далее на NAD + . В результате окислительного декарбоксилирования пирувата образуются ацетил-СоА, С02 и NADH.
Дальнейшее окисление ацетил-СоА осуществляется в ходе циклического процесса. Цикл Кребса начинается с взаимодействия ацетил-СоА с енольной формой щавелевоуксусной кислоты. В этой реакции под действием фермента цитратсинтазы образуется лимонная кислота. Следующий этап цикла включает две реакции и катализируется ферментом аконитазой, или аконитатгидратазой. В первой реакции в результате дегидратации лимонной кислоты образуется цис-аконитовая. Во второй реакции аконитат гидратируется и синтезируется изолимонная кислота. Изолимонная кислота под действием NAD- или NADP-зависимой изоцитратдегидрогеназы окисляется в нестойкое соединение — щавелевоянтарную кислоту, которая тут же декарбоксилируется с образованием а-кетоглутаровой кислоты (а-оксоглутаровой кислоты).
а-Кетоглутарат, подобно пирувату, подвергается реакции окислительного декарбоксилирования. а-Кетоглутаратдегидрогеназный мультиэнзимный комплекс сходен с рассмотренным выше пируватдегидрогеназным комплексом. В ходе реакции окислительного декарбоксилирования а-кетоглутарата выделяется С02, образуются NADH и сукцинил-СоА.
Подобно ацетил-СоА, сукцинил-СоА является высокоэнергетическим тиоэфиром. Однако если в случае с ацетил-СоА энергия тиоэфирной связи расходуется на синтез лимонной кислоты, энергия сукцинил-CoA может трансформироватся в образование фосфатной связи АТР. При участии сукцинил- СоА-синтетазы из сукцинил-СоА, ADP и Н3Р04 образуются янтарная кислота (сукцинат), АТР, регенерирует молекула СоА. АТР образуется в результате субстратного фосфорилирования.
На следующем этапе янтарная кислота окисляется до фумаровой. Реакция катализируется сукцинатдегидрогеназой, коферментом которой является FAD. Фумаровая кислота под действием фумаразы или фумаратгидратазы, присоединяя Н20, превращается в яблочную кислоту (малат). И, наконец, на последнем этапе цикла яблочная кислота с помощью NAD- зависимой малатдегидрогеназы окисляется в щавелевоуксусную. ЩУК, которая самопроизвольно переходит в енольную форму, реагирует с очередной молекулой ацетил-СоА и цикл повторяется снова.
Следует отметить, что большинство реакций цикла обратимы, однако ход цикла в целом практически необратим. Причина этого в том, что в цикле есть две сильно экзергонические реакции — цитратсинтазная и сукцинил-СоА-синтетазная.
На протяжении одного оборота цикла при окислении пирувата происходит выделение трех молекул С02, включение трех молекул Н2О и удаление пяти пар атомов водорода. Роль Н2О в цикле Кребса подтверждает правильность уравнения