Наследственные заболевания обмена веществ
НАСЛЕДСТВЕННЫЕ БОЛЕЗНИ ОБМЕНА ВЕЩЕСТВ
К настоящему времени известно более 2500 наследственных ферментопатий, 20 классов наследственных болезней обмена, но только для части из них (для 300) установлен точный уровень метаболического блока и характер ферментативного дефекта. До сих пор большая часть этих заболеваний не диагностируется или выявляется поздно, когда происшедшие нарушения носят необратимый характер. Одна из трудностей ранней диагностики заключается в том, что в период новорожденности у этих детей нет специфических расстройств, а поздние проявления фенотипически схожи с заболеваниями ненаследственного генеза. Вторая особенность состоит в том, что для наследственных заболеваний обмена веществ характерен клинический полиморфизм, обусловленный генетической гетерогенностью. Это объясняется наличием множественных изоаллельных мутаций и возможностью возникновения мутаций в разных генах.
Клинические проявления наследственных болезней обмена веществ во многом определяются поражением нервной системы (особенно при нарушениях обмена аминокислот, липидов и кислых гликозамино-гликанов), что в свою очередь, усиливает имеющиеся нарушения и усугубляет тяжесть клинических проявлений заболевания. Для диагностики наследственных болезней важен анализ неврологических симптомов, особенно на ранних стадиях развития, и разграничение их от фенокопий- заболеваний ненаследственной природы со сходной клинической картиной. Важное практическое значение имеет выявление гетерозиготных носителей мутантного гена при наследственных болезнях. Например, при частоте фенилкетонурии 1:10 000, мутантный ген встречаетсяв популяции 1:50. Гетерозиготное состояние может клинически не обнаруживаться, поэтому выявление умеренно выраженных изменений метаболизма является единственным указанием на наличие мутантного гена.
Наследственные болезни обмена аминокислот
Роль аминокислот для организма человека чрезвычайно велика. Аминокислоты являются основными структурными элементами белков, необходимы для синтеза иммуноглобулинов, гормонов, служат источником энергии. Каждый фермент или белок имеет специфические свойства и функции, которые определяют и регулируют сложные обменные процессы и развитие организма.
Часть аминокислот не может синтезироваться в организме человека. Это незаменимые аминокислоты: триптофан, фенилаланин, метионин, лизин, лейцин, изолейцин, валин и треонин. В детском возрасте к их числу относится гистидин, т.к. организм ребенка не может синтезировать эту аминокислоту в необходимых для нормального роста количествах. Клетки растущих тканей содержат аминокислоты в высоких концентрациях, что является свидетельством высокой интенсивности процессов транспорта аминокислот через клеточные мембраны.
Для обеспечения нормального роста и развития важно не только количество поступающих аминокислот, но и их соотношение. При избытке или недостатке аминокислот развиваются явления аминокислотного дисбаланса. Например, избыток лейцина в пище тормозит рост организма, метионина- вызывает токсическое поражение нервной системы, цистина- способствует развитию жировой инфильтрации печени.
Таким образом, нарушения метаболизма аминокислот приводят к нарушению нормального функционирования организма человека.
Наследственные нарушения обмена аминокислот
(Ю.И. Барашнев, Ю.Е. Вельтищев, 1978 г.)
1. Наследственные нарушения обмена аминокислот, сопровождающиеся увеличением их концентрации в крови и моче: фенилкетонурия, гистидинемия, триптофанурия, болезнь "кленового сиропа", орнитинемия, цитруллинемия и др. Наследование, в основном, по аутосомно-рецессивному типу. В основе развития заболеваний лежит нарушение синтеза или структуры тех или иных ферментов.
2. Наследственные нарушения обмена аминокислот, сопровождающиеся увеличением их выделения с мочой без изменения уровня в крови: гомоцистинурия, гипофосфатазия, аргиносукцинатацидурия и др. При данных энзимопатиях нарушено обратное всасывание в почках, что приводит к увеличению их содержания в моче.
3. Наследственные нарушения систем транспорта аминокислот: цистинурия, триптофанурия, болезнь Гартнепа и др. К этой группе относятся энзимопатии, развитие которых обусловлено снижением реабсорбции аминокислот в почках и кишечнике.
4. Вторичные гипераминоцидурии: синдром Фанкони, фруктоземия, галактоземия, болезнь Вильсона-Коновалова и др. При данных состояниях возникает вторичная генерализованная гипераминоацидурия в результате вторичных тубулярных нарушений.
Фенилкетонурия (ФКУ)
Впервые описана в 1934 г. Folling под названием "фенилпировиноградная имбецильность". Тип наследования - аутосомнорецессивный. Частота заболевания составляет 1:10000- 1:20000 новорожденных. Пренатальный диагноз возможен при использовании генетических зондов и биопсии ворсин хориона.
К развитию классической клинической картины при ФКУ приводит недостаточность фенилаланингидроксилазы и недостаточность редуктазы дигидроптерина- 2-го фермента, обеспечивающего гидроксилирование фенилаланина. Их недостаток приводит к накоплению фенилаланина (ФА) в жидких средах организма (схема 1). Как известно, ФА относится к незаменимым аминокислотам. Поступающий с продуктами питания и не используемый для синтеза белка, он распадается по тирозиновому пути. При ФКУ наблюдается ограничение превращения ФА в тирозин и, соответственно, ускорение его превращения в фенилпировиноградную кислоту и другие кетоновые кислоты.
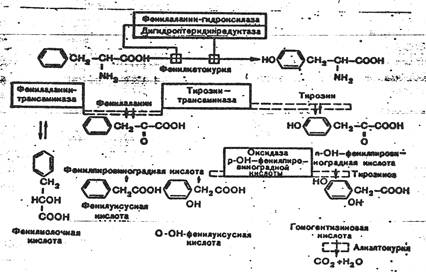
Схема 1. Варианты нарушений метаболизма фенилаланина.
Существование различных клинико-биохимических вариантов ФКУ объясняется тем, что фенилаланингидроксилаза является частью мультиферментной системы.
Различают следующие формы ФКУ:
1. Классическая
2. Скрытая.
3. Атипичная.
Развитие атипичных и скрытых форм ФКУ связывают с недостаточностью фенилаланинтрансаминазы, тирозинтрансаминазы и оксидазы парагидроксифенилпировиноградной кислоты. Атипичная ФКУ обычно не сопровождается поражением нервной системы в результате позднего развития ферментативного дефекта.
У женщин с фенилкетонурией возможно рождение детей с микроцефалией, задержкой умственного развития, нарушениями развития мочевыделительной системы, поэтому необходимо назначение диетотерапии во время беременности.
Клинические симптомы у больных ФКУ
При рождении ребенок с фенилкетонурией выглядит здоровым. Заболевание у этих детей проявляется на первом году жизни.
1. Интеллектуальный дефект. Нелеченный ребенок теряет около 50 баллов IQ к концу 1-го года жизни. У больных не выявляется зависимости между уровнем ФА и степенью интеллектуального дефекта.
2. Судорожный синдром (4 50%), экзема, гипопигментация.
3. Нарушение координации движения.
4. Задержка развития статических и двигательных функций.
5. Поражение пирамидных путей и стриопаллидарной системы. Клинические проявления классической ФКУ редко встречаются в странах, в которых действует программа неонатального скрининга на это заболевание.
У детей с фенилкетонурией наблюдается повышенный уровень в моче метаболитов ФА. Увеличение в физиологических жидкостях содержания ФА и недоокисленных продуктов его метаболизма приводит к поражению нервной системы. Определенная роль в этих нарушениях принадлежит дисбалансу аминокислот (дефицит тирозина, который в норме активно участвует в построении белкового компонента миелина). Демиелинизация является характерным патоморфологическим признаком фенилкетонурии. Нарушение соотношения аминокислот в
крови приводит к нарушению уровня свободных аминокислот в головном мозге, что вызывает слабоумие, гиперкинезы и другие неврологические симптомы.
Пирамидные симптомы обусловлены нарушением процессов миелинизации. Избирательный характер поражения нервной системы объясняется особенностями миелинизации- поражаются наиболее молодые в филогенетическом отношении отделы, выполняющие сложные и дифференцированные функции. С недостаточным образованием меланина из тирозина связывают голубой цвет глаз, светлую кожу. Запах "плесени" ("мышиный", "волчий") объясняется наличием фенилуксусной кислоты в моче. Кожные проявления (экссудативный диатез, экземы) связаны с выделением аномальных метаболитов. Недостаточность образования адренергических гормонов из тирозина приводит к артериальной гипотонии.
Необходимо отметить, что при ФКУ в патологический процесс вовлекается печень, но характер морфологических расстройств не является специфичным: выявляются признаки тканевой гипоксии, нарушения окислительной и белоксинтезирующей функции, перегрузка липидами. Наряду с этим наблюдаются компенсаторно-приспособительные изменения: высокое содержание гликогена, гиперплазия митохондрий. Генерализованную гипераминоацидемию при ФКУ можно объяснить вторичным нарушением метаболизма аминокислот в связи с повреждением гепатоцитов, т.к. многие ферменты, участвующие в аминокислотном обмене, локализуются в печени.
У нелеченых больных с классической ФКУ наблюдается значительное снижение концентрации катехоламинов, серотонина и их производных в моче, крови, ликворе. Поэтому в комплексном лечении ФКУ необходима промедиаторная коррекция, так как парциальный интеллектуальный дефект может быть связан с нейромедиаторными нарушениями.
Критерии диагностики классической формы фенилкетонурии:
1. Уровень ФА в плазме выше 240 ммоль/л.
2. Вторичный дефицит тирозина.
3. Повышенный уровень в моче метаболитов ФА.
4. Сниженная толерантность к полученному внутрь ФА.
Методы диагностики фенилкетонурии:
1. Проба Феллинга с FeCl3- при положительном анализе появляется сине-зеленое окрашивание мочи.
2. В крови выявление избытка фенилаланина возможно с помощью бактериального экспресс- теста Гольдфарба или теста Гатри (т.к. в течение первых дней жизни фенилпировиноградная кислота в моче может отсутствовать).
При ФКУ проводится лечение диетой с ограниченным содержанием ФА (главным образом назначают овощные блюда, мед, фрукты). Такие продукты, как молоко, молочные изделия, яйца, рыба, должны быть полностью исключены в период пребывания больных с ФКУ на острой диете. Назначаются специальные препараты (цимогран, лофеналак) и витамины.
Оптимальные сроки обследования новорожденных- 6-14 день жизни, начало терапии - не позднее 21 дня жизни. Необходимо помнить, что проведение исследования в первые сутки не исключает ложноположительных или ложноотрицательных результатов ( повторное исследование проводят до 21 дня жизни ). Эффективность лечения оценивается по интеллектуальному уровню развития пациента. Необходимо отметить, что лечение, начатое после года не нормализует интеллект полностью (возможно, это связано с развитием необратимых изменений в мозге).
ГОМОЦИСТИНУРИЯ
Заболевание впервые описано в 1962 г. Carson и Neil. Наследуется по аутосомно-рецессивному типу. Частота гомоцистинурии составляет 1:200 000 новорожденных.
В основе заболевания лежит отсутствие или снижение активности фермента цистатионинсинтетазы, что ведет к нарушению обмена метионина. Кофактором цистатионсинтетазы является витамин В6. Поэтому наблюдается пиридоксинчувствительная и пиридоксинрезистентная формы. У родителей и родственников больных часто обнаруживают шизофрению. Рядом авторов отмечается фенотипическое сходство с болезнью Марфана. Однако, при гомоцистинурии в отличие от болезни Марфана более выражены изменения нервной системы, снижение интеллекта и судорожный синдром.
Формы гомоцистинурии:
1. Классическая.
2. Связанная с дефицитом утилизации витамина В6.
3. Обусловленная нарушением метаболизма фолиевой кислоты.
Клинически дети, больные классической формой, при рождении выглядят здоровыми. Возможны лишь задержка роста и развития. Диагноз обычно устанавливается после 3-х лет, когда выявляется подвывих хрусталика. Основной рентгенологический признак- генерализованный остеопороз. При гомоцистинурии наблюдается клинический полиморфизм. Однако, можно выделить своеобразный комплекс признаков (таблица 1).
Таблица 1. Симптомокомплекс гомоцистинурии
( Ю.И.Барашнев, Ю.И.Вельтищев, 1978 г.)
| Симптомы | Фенотипические проявления |
| Изменение скелета | Укороченное туловище,удлиненные конечности, нарушенная осанка, "башенная" форма черепа, неправильный прикус и рост зубов,высокое небо, "крыловидные" лопатки, воронкообразная деформация грудной клетки, вальгусная деформация грудной клетки, вальгусная деформация нижних конечностей, плоскостопие, умеренный остеопороз |
| Изменение нервной системы | Сниженный интеллект,патологический характер ЭЭГ, спастическая походка |
| Нарушение зрения | Подвывих хрусталиков, вторичная глаукома, изменения глазного дна |
| Сердечно- сосудистые расстройства | Нарушение обменных процессов в миокарде (по данным ЭКГ) |
| Внешние признаки | Светлые, мягкие,вьющиеся крупными завитками волосы, голубой цвет радужной оболочки |
Гомоцистинурия ведет к поражению соединительной ткани за счет усиления синтеза сульфатированных протеогликанов с последующей дегенерацией эластических элементов, депозицией коллагена и кальцификацией. Вовлечение в патологический процесс соединительной ткани приводит к костным деформациям, подвывиху хрусталика книзу. Генез подвывиха хрусталика следующий: дефицит цистина приводит к вовлечению в процесс соединительнотканных волокон цинновых связок. У больных с гомоцистинурией выявляются разнообразные поражения органа зрения: близорукость, изменения глазного дна, вторичная глаукома. Резкое падение остроты зрения приводит к инвализации больных.
При гомоцистинурии с мочой избыточно выводится гомоцистин в результате инактивации цистатионинсинтетазы в головном мозге и печени больных. Изменения ЦНС у детей с гомоцистинурией обнаруживаются в 50 % случаев. Происхождение интеллектуального дефекта при этом заболевании до сих пор не ясно. Отмечено сочетание гомоцистинурии с эпилепсией, шизофренией, задержкой интеллектуального развития. Высказываются предположения, что основной причиной умственного дефекта при гомоцистинурии являются сосудистые мозговые тромбы, в связи с чем образуется много мелких инфарктов мозга. При этом возникают некротические и дегенеративные изменения в мозговом стволе, зрительном бугре и коре.
У больных более старшего возраста (до 30 лет) наблюдается склонность к артериальным и венозным тромбозам, что связано с активацией гомоцистином фактора Хагемана, а также с оседанием гомоцистина из-за его низкой растворимости в патологически измененной интиме сосудов. Оба этих процесса могут создавать условия для образования тромбов.
Необходимо отметить, что гомоцистинурии свойственен прогредиентный характер течения патологического процесса. При рождении дети обычно не имеют каких-либо внешних дефектов. Но в результате наследственных нарушений постепенно начинают выявляться изменения в отдельных органах и системах. Существует зависимость клинической картины от возраста. Чем старше ребенок, тем больше органов и систем вовлекается в патологический процесс. Таким образом, гомоцистинурия - это заболевание всего организма. Диагностическим признаком является избыточная экскреция с мочей гомоцистина (необходима свежесобранная моча, т.к. гомоцистин разрушается при хранении).
ГИСТИДИНЕМИЯ
Заболевание впервые описано в 1961 г. Ghadimi с соавторами, а термин "гистидинемия" предложен Auerbach с соавт. в 1962 году.
Заболевание возникает в результате отсутствия или недостаточности активности фермента гистидазы. Наследуется аутосомно-рецессивно. Высказывается мнение об аутосомно-рецессивной передаче с неполной пенетрантностью, сцепленном с Х-хромосомой наследовании. Т.е., возможно, различные формы гистидинемии наследуются по разному. Для детей первого года жизни гистидин - незаменимая аминокислота. При недостатке гистидина в этом возрасте отмечается нарушение ретенции азота, выявляется дефицит массы тела, появляется шелушение кожи и экзематозные высыпания. Существует точка зрения о незаменимости гистидина и для здоровых взрослых (при недостатке наблюдаются признаки анемии с нарушением эритропоэза).
При гистидинемии происходит нарушение самого эффективного активного пути катаболизма- превращение гистидина в уроканиновую кислоту (этим путем в норме катаболизируется большая часть гистидина). В результате метаболического блока происходит накопление в крови и моче гистидина. Увеличение активности трансаминирования и усиленный перевод гистидина в имидазолпировиноградную, имидозолмолочную и имидозолуксусную кислоты является компенсаторно-приспособительной реакцией организма.
Гистидинемия отличается большой вариабельностью клинических проявлений: от тяжелой умственной отсталости до полного отсутствия каких-либо симптомов. Снижение интеллекта выявляется лишь у 50 % больных детей. Больные гистидинемией имеют светлый цвет волос, голубые глаза. На первый план у таких детей выступает поражение нервной системы: снижение интеллекта, нарушение речи, судороги. А у детей с нормальным интеллектом можно выявить особенности психики при гистидинемии: эмоциональную лабильность, агрессивность. Характер повреждения нервной системы при данном заболевании зависит от степени инактивации гистидидазы. Иногда гистидинемия сочетается с аномалиями развития, патологией почек, костной системы.
Для диагностики заболевания необходимо выявление повышенного уровня гистидина в плазме. Окончательный диагноз подтверждает определение гистидидазы в ороговевающем эпителии или печени.
Наследственные нарушения обмена триптофана
Как известно, триптофан является незаменимой аминокислотой.
Образующийся при расщеплении белков триптофан через кишечную стенку всасывается в кровь и используется организмом для синтеза белков. Остальная часть идет на синтез биологически активных веществ: никотинамида, серотонина, мелатонина и др. Таким образом, процессы метаболизма триптофана идут по трем основным направлениям: серотониновому, индольному и кинурениновому.
К наследственно обусловленным нарушениям обмена триптофана относится ряд клинических синдромов и заболеваний:
1. Болезнь Гартнепа.
2. Индиканурия.
3. Синдром Тада.
4. Синдром Прайса.
Болезнь Гартнепа
Впервые описана Baron с соавт. в 1956 году. Аутосомно- рецессивный тип наследования. При данном заболевании наблюдается генетическое изменение транспортной функции клеток слизистой оболочки кишечника и проксимальных отделов почечных канальцев. Это ведет к изолированному дефекту транспорта моноаминокарбоновых кислот. Нарушение кишечной абсорбции триптофана приводит к его бактериальному расщеплению в кишечнике до индола и индоксила. Генерализованная аминоацидурия обусловлена нарушением канальцевой реабсорбции.
Для болезни Гартнепа характерны кожная фоточуствительность, пеллагроподобный дерматит, мозжечковая атаксия с вовлечением в процесс пирамидных путей, нарушение функции желудочно-кишечного тракта. У некоторых детей выявляется умственная отсталость.
Индиканурия
Впервые описана в 1965 году Bickel.
В основе заболевания лежит нарушение всасывания триптофана в кишечнике с образованием избыточного количества индола, который всасывается, окисляется, сульфатируется и выделяется в виде индикана. Последний окисляется под влиянием воздуха до голубого индикана, окрашивающего пеленки в синий цвет (болезнь "голубых пеленок").
При индиканурии наблюдается гиперкальциемия, нефрокальциноз, периодическая гипертермия.
Синдром Тада
Данный синдром впервые описан в 1963 году Tada с соавт. под названием "триптофанурия с нанизмом". Аутосомно- рецессивный тип наследования. При синдроме Тада наблюдается недостаток фермента триптофанпирролазы, катализирующего превращение триптофана в кинуренин. Нарушения связаны с эндогенным дефицитом никотиновой кислоты и избытком индольных соединений. При синдроме Тада отмечается глубокая умственная отсталость, нанизм, мозжечковая атаксия.
Синдром Прайса
Впервые описан в 1967 г. Price с соавторами. Генетический дефект кинуренингидроксилазы. Наблюдается избыточное выделение с мочой кинуренина за счет блока фермента. Основное проявление синдрома Прайса - склеродермия.
Галактоземия
В 1908 году Reuss впервые отметил, что галактоземия относится к "врожденным ошибкам обмена". Изучению основного и побочного путей преобразования галактозы способствовали труды многих ученых.
Классическая галактоземия наследуется по аутосомно- рецессивному типу. По частоте занимает 2-е место после ФКУ. При этом заболевании наблюдается дефицит галактозо-1-фосфат-уридилтрансферазы. В эритроцитах гомозигот при классической галактоземии активность данного фермента почти не определяется, у гетерозигот составляет 50 % нормы.
Главный путь преобразования галактозы в глюкозу - это путь Лелуа. Первым этапом является фосфорилирование галактозы в печени, мозге, эритроцитах. В результате этой реакции образуется галактозо-1-фосфат, для дальнейшего превращения которого необходим специфический фермент галактозо-1-фосфат- уридилтрансфераза. При дефиците галактозо-1-фосфат - уридилтрансферазы невозможен дальнейший метаболизм галактозо-1-фосфата до УДФ- галактозы. Накопление галактозо-1-фосфата приводит к заболеванию, возможно, и во внутриутробном периоде. Кроме основного пути обмена галактозы (пути Лелуа), существуют обходные, дополнительные пути, которые необходимо учитывать в патологических условиях при дефиците галактозы.
Необходимо помнить, что из-за наличия большого числа фенокопий галактоземия не всегда распознается своевременно. Целый ряд болезней периода новорожденности клинически сходен с галактоземией: гемолитическая болезнь новорожденных, врожденный гепатит, атрезия желчных путей, энзимопатическая желтуха Криглера-Найяра и ряд других заболеваний.
При классической галактоземии наблюдается раннее появление симптомов заболевания: анорексия, рвота, непереносимость молока, задержка увеличения массы тела, катаракта, гепатомегалия, желтуха, отеки, геморрагические проявления, спленомегалия, поражение ЦНС. Задержка психомоторного развития выявляется рано и прогрессирует с возрастом (однако, умственная отсталость менее выражена, чем при ФКУ).
Тяжелые формы заболевания имеют яркую клиническую картину уже в первые дни жизни: расстройство пищеварения и резкая интоксикация (рвота, понос, гипотрофия), желтуха, которая имеет стойкий характер и наступает за счет увеличения концентрации прямого билирубина. Нередко печеночная желтуха сочетается с гемолитической за счет снижения осмотической резистентности эритроцитов. Необходимо отметить, что галактозо-1-фосфат является гепатотоксичным. Постепенно у больного прогрессируют признаки печеночной недостаточности. На 2-3 месяце жизни развивается асцит, спленомегалия, нарастают явления токсикоза и эксикоза. Повышенный уровень галактиола приводит к развитию катаракты (при тяжелой форме галактоземии катаракта может наблюдаться при рождении). Терминальная стадия болезни характеризуется печеночной недостаточностью, выраженной дистрофией и присоединением вторичных инфекций.
Диагностика заболевания основана на определении галактозы в крови и моче. Пренатальная диагностика- определение фермента в клетках амниотической жидкости. Тест на толерантность к галактозе не нужен и опасен, т.к. галактоза оказывает повреждающее действие.
Недостаточность лактазы
Под действием фермента лактазы в пищеварительном тракте человека происходит ферментативный гидролиз лактазы на глюкозу и галактозу. Существуют две разновидности фермента: "детского" и "взрослого" типа. Ген, контролирующий перевод лактазы "детского" типа во "взрослый", локализован на 2 хромосоме. В период до 5 лет происходит переключение синтеза фермента на "взрослый" тип. В некоторых случаях возможна персистенция "детской" лактазы во взрослом организме.
Формы лактазной недостаточности:
1. Алактазия- первичная наследственная лактазная недостаточность. Предполагаемый тип наследования аутосомно-рецессивный.
2. Транзиторная форма.
3. Гиполактазия взрослых.
4. Вторичная недостаточность лактазы.
Первичная недостаточность лактазы впервые описана A.Holzel в 1959г. Развивается тяжелая диспепсия, дегидратация, токсикоз и обезвоживание. Встречается редко, приводит к смерти в грудном возрасте.
Транзиторная недостаточность связана с незрелостью ферментов кишечника. В нормальных условиях активность кишечной лактазы возрастает на 24-40 неделе беременности. У недоношенных эта форма лактазной недостаточности проявляется поносом, рвотой, дегидратацией.
Взрослый тип чаще встречается у негров, индейцев и др. этнических групп. Среди русских- у 10-20 %. Клинически, как правило, не выявляется. Связан с персистенцией лактазы "детского" типа в результате мутации регуляторного гена.
Вторичная недостаточность лактазы может развиться при тяжелых расстройствах пищеварения, кишечных дисбактериозах, пищевой аллергии, лямблиозе, аскаридозе.
У детей с лактазной недостаточностью нарушается водно-солевое равновесие за счет повышенного выведения с мочой калия и кальция. Потеря кальция может привести к задержке оссификации хрящевой ткани у детей.
Лечение заключается в соблюдении безлактазной диеты. Эффективно применение фермента лактазы.
Врожденные нарушения обмена гликогена
Гликоген является важнейшим биополимером и содержится во всех клеточных органеллах. Этот полисахарид служит основным источником энергии и является резервом углеводов в организме.
В норме гликоген непрерывно подвергается обменным реакциям. В его синтезе и распаде участвует множество ферментов. Нарушение какого-либо звена в общей системе ферментов приводит либо к аномальному накоплению гликогена в клетках, либо к истощению его запасов. Врожденные нарушения в обмене гликогена могут возникать во всех органах (генерализованное заболевание) или в одном органе (чаще в мышцах или печени). Симптомы заболевания, вызванные одним и тем же ферментным дефицитом, могут проявляться в любом возрасте. В связи с этим различают инфантильную, юношескую и взрослую формы заболевания. Наиболее тяжелыми являются генерализованные заболевания инфантильной формы.
Необходимо отметить, что классификация гликогеновой болезни по формам заболевания, основанная на клинических данных, является рабочей классификацией клиницистов. В настоящее время принята классификация гликогенозов, предложенная Cori и основанная на ферментом дефекте заболевания (таблица 2).
Таблица 2 Болезни, вызванные нарушением обмена гликогена.
| Тип гликогеноза (название болезни) | Неактивный фермент | Органы, ткани и клетки, в которых найден дефект фермента | Клиническая форма болезни |
| I (болезнь Гирке) | Глюкозо-6 фосфатаза | Печень, почки,слизистая тонкого кишечника | Печеночная |
| II(болезнь Помпе) | Кислаяa глюкозидаза | Печень, почки,селезенка мышцы, лейкоциты, нерв ная ткань | Генерализованная |
| III(болезнь Кори) | Амило-1,6- глюкозидаза | Печень, мышцы, лейкоциты, эритроциты | Печеночная, мышечная |
| IV(болезнь Андерсона) | Ветвящий фермент | Печень, мышцы, лейкоциты | Печеночная |
| V (болезнь Мак-Ардля) | Фосфорилаза мышц | Мышцы | Мышечная |
| VI(болезнь Херса) | Фосфорилаза печени | Печень | Печеночная |
| VII(болезнь Томсона | Фосфоглюкомутаза | Мышцы, печень | Мышечная, Печеночная |
| VIII(болезнь Таруи) | Фосфофруктокиназа | Мышцы, эритроциты | Мышечная |
| IХ(болезнь Хага) | Киназа фосфорилазы b | Печень | Печеночная |
| Х | Протеинкиназа | Печень | Печеночная |
| ХI | Фосфогексоизомераза | Печень, эритроциты | Печеночная |
Гликогеноз I типа
Описан в 1952 г. C.Cori и G.Cori. Заболевание наследуется по аутосомно- рецессивному типу. Дефект фермента глюкозо-6-фосфатазы.
В зависимости от дефекта компонентов глюкозо-6-фосфатазной системы, различают три подтипа I типа гликогенозов: IА, IВ и IС.
IА - болезнь Гирке ( гепаторенальный гликогеноз) вызван отсутствием активности специфической глюкозо-6-фосфатазы в печени, слизистой кишечника, почках (скелетная и сердечная мускулатура, лейкоциты в процесс не вовлекаются, т.к. в нормальных условиях в этих тканях отсутствует глюкозо-6-фосфатаза).
IВ- связан с дефектом транспорта этого фермента в микросомальных мембранах гепатоцитов.
IС- транспортный дефект неорганического фосфата на уровне микросомальных мембран.
Глюкозо-6-фосфатазе принадлежит центральная роль в нормальном гомеостазе глюкозы. Она обеспечивает образование более 90 % глюкозы, освобождаемой в печени. При болезни Гирке нарушена одна из важнейших функций печени- поддержание гомеостаза глюкозы крови. Кроме этого нарушен процесс образования глюкозы из аминокислот. Развивающийся обменный дисбаланс приводит к гипогликемии, гиперлактатемии, накоплению гликогена в гепатоцитах. Причиной гипогликемии и увеличения образования лактата являются отсутствие гидролиза Гл-6-Ф и усиление обмена гексозофосфатов в цикле Эмбдена-Мейергофа. Гл-6-Ф накапливается в ткани печени, активирует гликогенсинтетазу и вызывает накопление в печени гликогена, нормального по структуре. В гепатоцитах выявляется большое количество липидов. Нарушение обмена липидов проявляется повышением уровня триглицеридов в крови. Вследствие нарушения энергообеспечения процессов реабсорбции в канальцах почек наблюдаются глюкозурия и аминоацидурия.
Клинические симптомы появляются в 1-й год жизни: маленький рост, "кукольное лицо" (за счет отложения жира в области щек), гипотрофия, гепатомегалия и умеренное увеличение почек. Умственное развитие, как правило, не страдает. Гипогликемия является основным ведущим клиническим симптомом этого типа гликогенозов.
Особенность этого типа гликогенозов: у детей в возрасте 5-7 лет возникают частые носовые кровотечения, геморрагические высыпания, а также гиперурикемия.
Гликогеноз II типа
Открыт H.-G. Hers в 1963 году. Тип наследования аутосомно-рецессивный. Наблюдается дефект фермента кислой a-глюкозидазы.
Это заболевание относится к лизосомальным болезням. При гликогенозе II типа практически во всех органах больного отсутствует активность кислой a-глюкозидазы. Этот фермент расщепляет a-1,4- и a-1,6 связи в молекуле гликогена. При дефекте фермента в лизосомах происходит аномальное накопление гликогена. Эти аномальные лизосомы служат морфологическими маркерами. Болезнь Помпе- единственная лизосомальная болезнь из гликогенозов, остальные гликогенозы связаны с дефектами ферментов, локализованных в цитоплазме.
Заболевание чрезвычайно гетерогенное. Различают инфантильную форму (болезнь Помпе), юношескую и взрослую формы. Каждая из форм гликогеноза II типа неоднородна в связи с существованием различным вариантов дефекта в синтезе или процессинге фермента.
Генерализованная форма заболевания - болезнь Помпе (инфантильная форма гликогеноза II типа, гликогеноз типа IIа). При болезни Помпе с 1-го года жизни наблюдается симптомокомплекс сердечной недостаточности. Поэтому этот тип заболевания часто называют "сердечным гликогенозом". У больного выявляется "шаровидное" сердце, умеренная гипертрофия мышц, увеличение печени, прогрессирующая мышечная слабость. Гипертрофия мышечных волокон сопровождается большим накоплением гликогена. Смерть на 1-ом или 2-ом году от сердечной недостаточности и респираторных заболеваний. При патологоанатомическом исследовании обнаруживают гипертрофию миокарда без органического поражения клапанов.
При гликогенозе II типа наблюдается накопление гликогена не только в печени, скелетных и сердечной мышцах, но и в легких, селезенке, гипофизе, надпочечниках, диафрагме, мозге, в тканях глаза. Структура гликогена при этом не отличается от нормы. Гликоген может находится в лизосомах (аномальные лизосомы) или же свободно лежать в цитоплазме гепатоцитов при разрушении лизосом. Единственным органом, в котором не обнаруживается значительное накопление гликогена, являются почки (в них имеется особый нейтральный фермент, активный в кислых условиях).
При юношеской форме наблюдается дефицит активности a-глюкозидазы в мышцах. Смерть наступает в результате осложнений респираторного характера.
При взрослой форме заболевание напоминает прогрессирующую мышечную дистрофию Дюшена. Клинические симптомы менее выражены, у больных поражаются только скелетные мышцы.
Особенность гликогеноза II типа- отсутствие у больных нарушений обмена. Это связано с тем, что фосфорилазная система не нарушена. Пренатальный диагноз основан на обнаружении вакуолизированного гликогена в амниотической жидкости и исследовании активности фермента в биоптатах хориона.
Гликогеноз III типа
(Болезнь Кори, болезнь Форбса, лимитдекстриноз)
Наследуется по аутосомно- рецессивному типу.
Это заболевание вызывается полным отсутствием или снижением активности амило-1,6- глюкозидазы- фермента, расщепляющего a- 1,6- глюкозидные связи в точках ветвления гликогена.
Дефект данного фермента приводит к образованию аномального по структуре и свойствам гликогена- лимитдекстрина, сходного по структуре с декстрином. Лимитдекстрин имеет укороченные концевые ветви молекул. Аномальный гликоген накапливается в печени и является "инертным" для обмена. При гистохимическом исследовании гепатоцитов обнаруживают их жировую инфильтрацию и накопление полисахаридов в цитоплазме. При световой микроскопии печени выявляют ядерный гликогеноз с небольшим количеством внутриклеточных включений. Необходимо отметить, что амило-1,6 глюкозидаза имеет 2 ферментативные активности: трансферазную и гидролитическую. Такая сложность функций фермента является причиной существования различных форм заболевания (генерализованная и локализованная). Синтез данного фермента в печени и мышцах контролируется различными генами, поэтому при нарушении ферментативной активности лимитдекстрин накапливается только в печени или в мышцах (в саркоплазме, между миофибриллами). Нарушение процесса распада гликогена сопровождается активацией компенсаторных механизмов. Активизируется распад белков, образуются глюкогенные и кетогенные аминокислоты.
Наиболее тяжелые проявления гликогеноза II типа наблюдаются при генерализованной форме.
Клинические проявления гликогенеза III типа: гепатомегалия, задержка физического развития (без нарушения интеллекта), гипогликемия натощак, т.е. клиническая картина у детей часто напоминает болезнь Гирке. Заболевание протекает д