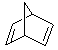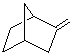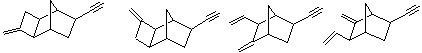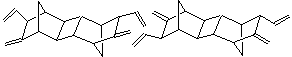Норборненна-2,5-диен и его свойства
Список используемых сокращенийНБН, нор – С7Н10 – норборнен – 2, бицикло (2.2.1) гепт –2 – ен
НБД, нор – С7Н8 – норборнадиен – 2,5, бицикло (2.2.1) гепта –2,5 – диен
ЦПД – циклопентадиен – 1,3
АА – аллилацетат
АФ – аллилформиат
БАН – бис(η3-аллил) никель
acac – ацетилацетон
Ме – метил
Et – этил
Pr – пропил
Bu – бутил
Ph – фенил
all – аллил
Введение
Норборненна- 2,5-диен (НБД) или бицикло (2.2.1) гептан-2,5-диен и его производные приобретают все большее значение в различных сферах человеческой деятельности, появляются все новые области их использования. Эти соединения нашли применение в медицине, сельском хозяйстве, ракетной технике, в производстве полимерных материалов с уникальными свойствами, микроэлектронике и в качестве конверторов солнечной энергии. Количество патентов, связанных с получением и применением производных НБД и норборнена-2 (НБН) достигает 10 тыс.
Исключительно важным является то обстоятельство, что сам НБД и некоторые его простейшие производные имеют надежную сырьевую базу. Это крупнотоннажные продукты нефтепереработки: циклопента-1,3-диен (ЦПД), ацетилен, алкены и алкадиены различного строения. Производство ЦПД может легко сочетаться с производством других продуктов нефтепереработки, в частности этилена.
Чрезвычайно интересными и привлекательными в отношении реакций с участием НБД и НБН-производных представляются возможности металлокомплексного катализа.
Реакции циклоприсоединения с участием НБД являются наиболее интересными и перспективными для практического использования. Несмотря на большое количество работ в этом направлении, синтетические возможности НБД в такого рода превращениях далеко не исчерпаны.
Реакция каталитического аллилирования НБН впервые описана в работе M. Catellani и G. Chiusoli в 1979 году. Необычный характер ее протекания связан не только с образованием интересных карбоциклических структур, но и возможностью активации С-С и С-Н – связей в мягких условиях.
Необычность реакции заключается в характере присоединения аллильной группы – не традиционным, а циклическом и даже с разрывом С – С-связи.
Катализируемое аллильное алкилирование норборненовых НБД и НБН – производных позволяет в одну технологическую стадию получить сложные полициклические углеводороды, содержащие метиленциклобутеновый фрагмент или метиленовую и винильную группы.
Дальнейшее развитее и усовершенствование методов металлокомплексного катализа применительно к реакции аллилирования НБД и его производных, детальное изучение механизма процесса, несомненно, приведут к увеличению выхода и селективности уникальных продуктов, сделают их производство технологичным и экономически оправданным.
Глава 1. Литературный обзор
 Норборненна - 2,5-диен 1 (бицикло (2.2.1) гептан-2,5-диен) (НБД) является бициклическим диеновым углеводородом норборненового ряда. Впервые он был получен в 1951 г. По реакции диенового синтеза из циклопента-1,3-диена и ацетилена.
Норборненна - 2,5-диен 1 (бицикло (2.2.1) гептан-2,5-диен) (НБД) является бициклическим диеновым углеводородом норборненового ряда. Впервые он был получен в 1951 г. По реакции диенового синтеза из циклопента-1,3-диена и ацетилена.
1
Наличие в молекуле НБД метиленового мостика, "стягивающего" С1 - и С4 - атомы приводит к цисоидному напряжению сжатия и значительному искажению валентных углов, а следовательно, и к повышению внутренней энергии молекулы.
Расстояния между атомами углерода и валентные углы в молекуле НБД
| Расстояние, Å | Валентные углы, град. |
| С12 1,522 | С123 109,1 |
| С17 1,558 | С217 96,4 |
| С23 1,333 | С216 102,2 |
В первую очередь это сказывается на реакционной способности двойных связей, энергия напряжения в которых оценивается в 25 кДж/моль для НБН и в 58 кДж/моль для НБД (на две двойные связи). π-Электронные орбитали последнего взаимодействуют, что обуславливает их гомосопряжение и делает возможным участие НБД в реакции диенового синтеза в качестве как диена, так и диенофила. Таким образом, наличие двух внутрициклических двойных связей, обладающих повышенной реакционной способностью, и их гомосопряжение определяют основные свойства НБД.
Среди реакций НБД можно выделить основные группы: изомеризации (распада) и присоединения. Помимо этого НБД свойственны реакции окисления и полимеризации.
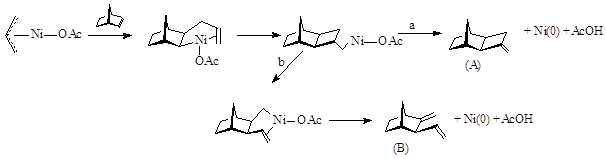 В 1979 году в работе Кателлани и сотр.1 впервые была показана возможность протекания реакции аллилирования НБН под действием комплексов никеля(0).
В 1979 году в работе Кателлани и сотр.1 впервые была показана возможность протекания реакции аллилирования НБН под действием комплексов никеля(0).
Схема
1.1. Механизм образования продуктов аллилирования НБН
Этот процесс включает гидридное элиминирование после встраивания молекулы субстрата по связи Ni – аллил. В присутствии НБН образуется интермедиат А cis, exo – строения. Далее происходит замыкание четырехчленного кольца (направление a), с образованием cis, exo продукта I, имеющего метиленциклобутановый фрагмент. Реакция может реализовываться по направлению b с образованием продукта II (exo), имеющего метиленовую и винильную группу.
Соотношение продуктов зависит от температуры: если при 800С А/В =3/7, то при 200С соотношение продуктов А и В равно 1/1.
Перераспределение водорода между η3-аллильными лигандами – наименее изученное направление превращения комплексов переходных металлов. Это свойство проявляется количественно в реакции Ni(C3H5) 2 с НБД, приводящей к широкой гамме продуктов окислительного аллилирования (I – III) и восстановления (СзН6) 10.
 |
Ni(C3H5) 2 + 3,3C7H8 → C10H12 + 0,3 C10H14 + 0,7 C3H6 + Ni(C7H8) 2 (1)
Указанные соединения образуются в результате присоединения к НБД аллильной группы, ранее принадлежавшей комплексу.
Взаимодействие Ni(C3H5) 2 с НБД протекает количественно при 25°С за несколько минут и сопровождается изменением окраски реакционного раствора. Желтый цвет, обусловленный Ni(СзН5) 3, переходит в темно-красный, характерный для олефиновых комплексов Ni(0). Интенсивность окрашивания пропорциональна исходной концентрации аллильного комплекса. При образовании темно-красных растворов существенно уменьшается концентрация НБД, расход которого составляет 3,3 моля на 1 моль Ni(C3H5) 2. Реакцию (1) удобно анализировать в виде суммы двух уравнений,
0,7 Ni(C3H5) 2 + 3C7H8 → С10Н12 + С3Н6 + Ni(C7H8) 2 (2)
0,3 Ni(C3H5) 2 + 4С7Н8 → С10Н12 + С10Н14 + Ni(C7H8) 2 (3)
относительный вклад которых составляет 0,7 и 0,3 соответственно.
Каждое уравнение формально описывает реакцию переноса атома водорода между аллильными лигандами. При этом более ненасыщенный фрагмент С3Н4 всегда входит в состав аддуктов С10Н12, в то время как фрагмент С3Н6 может находиться как в связанном состоянии (С10Н14), так и в виде пропилена. Суммарное количество пропилена и соединения С10Н14 эквимолярно сумме продуктов с брутто-формулой С10Н12.
Анализируя зависимость выхода продуктов I-III от мольного отношения НБД/NiA112, видно, что увеличение отношения до 10: 1 способствует образованию продукта восстановительного аллилирования. Дальнейший рост отношения практически не влияет на его выход, максимальное значение которого при данной температуре определяется природой комплекса. Прослеживается увеличение выхода I-III за счет С3Н6 (С4Н8) с ростом эффективного положительного заряда на никеле: Ni(2-CH3C3H4) 2> Ni(C3H5) > Ni(l-CH3C3H4) 2.
Температура в меньшей степени влияет на образование продуктов восстановительного аллилирования. Их выход незначительно падает с повышением температуры.
При исследовании влияния концентрации НБД на соотношение Сва/СAll+H было выяснено, что эта зависимость для всех комплексов никеля носит линейный характер, этот факт свидетельствует о более высоком кинетическом порядке по НБД для продуктов восстановительного аллилирования по сравнению с пропиленом или бутенами.
Общий характер диспропорционирования водорода между η3-аллильными лигандами подтвержден для комплексов различных переходных металлов Со, Fe, Ni, Rh, Pd и Pt. Из данных таблицы видно, что строение аддуктов определяется закономерностями, присущими и другим процессам циклоприсоединения с участием НБД 12313131. Так, при использовании комплексов никеля, палладия и платины образуются соединения, имеющие двойную связь в норбоненовом кольце. Этот факт предполагает монодентатный характер координации НБД в комплексах переходных металлов подгруппы никеля. Близость соотношений продуктов для этих металлов указывает на сходство их координационных возможностей. Однако активность комплексов в изучаемой реакции существенно уменьшается от никеля к платине, что связано с возрастанием эффективного положительного заряда металла в этом ряду.
Крайне неустойчивые комплексы Fе(С3Н5) 3 и Со(С3Н5) 3 активно взаимодействуют с НБД уже при температуре его плавления (-19°С). Помимо продуктов с НБН-фрагментом I – II в значительных количествах образуется соединение с нортрициклановой структурой III. Такой набор продуктов обусловлен большими координационными возможностями железа и кобальта по сравнению с переходными металлами подгруппы никеля. Подобным образом с НБД взаимодействует Rh(С3Н5) 3, однако его активность в исследуемой реакции существенно ниже.
Результаты балансовых и кинетических опытов, а также информация о строении образующихся продуктов позволяют высказать некоторые соображения о механизме взаимодействия Маlln с НБД (рис.1.1).
Механизм реакции основан на известных свойствах η3-аллильных комплексов: η3→ η1-изомеризации аллильных лигандов, внедрении ненасыщенных молекул по η1-связи металл-углерод, стадиях β-элиминирования и гидридного переноса, а также способности молекулы НБД как к монодентатной, так и хелатной координации.
Образование продуктов восстановительного аллилирования обусловлено координацией и внедрением второй молекулы НБД. При распаде общего комплекса в результате различных направлений протекания стадии гидридного переноса происходит формирование продуктов восстановительного аллилирования и С3Н6 (C4H8).
Образующийся после внедрения второй молекулы НБД координационно ненасыщенный комплекс должен быть крайне неустойчивым. Вследствие этого в аллилнорборненовом фрагменте не успевают произойти многочисленные превращения, имеющие место при внедрении первой молекулы НБД. В результате образуется только один продукт восстановительного аллилирования (C10H14) в отличие от широкого ассортимента соединений C10H12.

Рисунок 1.1. Механизм взаимодействия Мalln с НБД
Ключевая стадия – β-гидридный перенос - подтверждается хромато-масс-спектрометрическим исследованием продуктов модельных систем: Ni(C3D5) 2 – НБД и Ni(С3Н5) 2 – НБД-D8. Их строение указывает на участие в процессе атомов водорода, принадлежащих как НБД, так и аллильному фрагменту и занимающих β-положение по отношению к металлу (рис.1.2).
Предложенный механизм объясняет строение всех продуктов аллилирования НБД. Для каждого переходного металла характерен индивидуальный набор соединений и, следовательно, определенная совокупность стадий, приводящая к их образованию.
Так для Malln подгруппы никеля характерна совокупность стадий, объединенная общим направлением (а). Для комплексов железа, кобальта и родия реализуются оба направления: (а) - связанное с монодентатной координацией НБД в комплексе и (б) - проявляющееся при хелатной его координации.
Реакции окислительно-восстановительного диспропорционирования для различных субстратов (различные классы ненасыщенных соединений, отличающиеся природой и реакционной способностью кратной связи) могут быть разделены на три группы:
Реакция не идет (А)
Ni(C3H5) 2 + ненасыщенный углеводород Гексадиен-1,5 (Б)
Продукты аллилирования (В)
А. этилен, пропилен, пентен-1, пентен-2, 2-метиопентен-2, гексадиен-1,5, винилциклопропан, метиленциклобутан, циклопентен, циклогексен;
Б. аллен, бутедиен-1,3, метиленциклопропан, циклопентадиен-1,3, трансциклооктадиен-1,5;
В. Норборнадиен, норборнен и его 5,6-производные.
В первую группу входят соединения, не взаимодействующие с бис(π-аллил) никелем. Это линейные и циклические алкены, диены с изолированными двойными связями (гексадиен-1,5), а также соединения, у которых двойная связь примыкает к умеренно напряженному углеродному кольну (метиленциклобутан).
Во вторую группу соединений входят диеновые углеводороды с кумулированными (аллен) и сопряженными (бутадиен-1,3, циклопентадиен) двойными связями, а также олефины у которых двойная связь примыкает к напряженному углеродному кольцу (метиленциклопропан). Эти соединения вытесняют из бис(π-аллил) никеля гексадиен-1,5. При этом образуется π-комплекс никеля с соответствующим соединением, способный в ряде случаев катализировать его циклическую олигомеризацию.
Наконец, в третью группу входят НБД, НБН и его многочленные 5,6-производные.
Таким образом, субстратом для реакции аллилирования являются соединения с внутрициклической двойной связью.
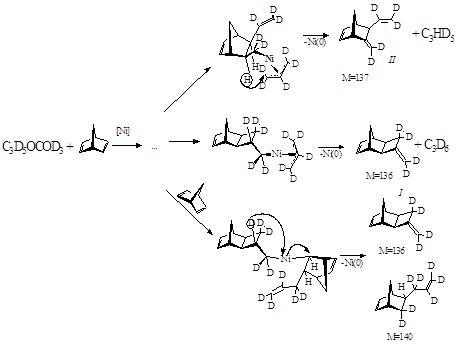 |
Анализ величин энергий напряжения двойных связей (табл.1.1) в циклоалкенах приводит к выводу, что уникальная реакционная способность двойных связей в НБД - и НБН-производных связана с внутримолекулярным напряжением углеродного каркаса. Эта энергия, частично высвобождающаяся при координации, полностью компенсирует затраты на только одного аллильного лиганда.
Рисунок 1.2. Фрагмент механизма для модельной системы Ni(C3D5) 2 – НБД.
Таблица 1.1. Энергия напряжения двойной связи в некоторых циклоалкенах и метиленциклоалканах.
| Субстрат | Напряжение двойной связи, кДж/моль | Субстрат | Напряжение двойной связи, кДж/моль |
| 58,2 (две связи) |
| 34,8 |
| 25,1 |
| 12,6 |
Продолжение.
| 15,5 |
| 11,4 |
| 9,6 |
| 8,1 |
| 0,8 |
Это условие, видимо, играет важнейшую роль для дальнейшего протекания процесса по пути окислительно-восстановительного диспропорционирования. Энергия напряжения двойной связи должна находиться в пределах 25-30 кД ж/связь. Следовательно, в реакции аллилирования могут вступать непредельные углеводороды имеющие напряженную внутрицеклическую двойную связь.
Таким образом, стехиометрическое взаимодействие может служить своего рода индикатором, указывающим на принципиальную возможность того или иного соединения вступать в реакцию каталитического аллилирования.
Гомогенно – каталитическое аллилирование НБД и НБН - производных.
Катализируемое аллильное алкилирование норборненовых (НБ) производных позволяет в одну технологическую стадию получить сложные полициклические углеводороды, содержащие метиленциклобутеновый фрагмент или метиленовую и винильную группы (реакция 4) 1:
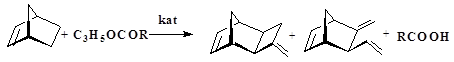
(4)
Катализаторами этой и родственных реакций являются системы на основе комплексных соединений никеля и палладия. Аллилирующими агентами служат сложные аллиловые эфиры органических кислот, среди которых наиболее часто используется аллилацетат. Аналогичные результаты могут быть полученны при использовании аллилпропионата, аллилбутирата или аллилбензоата (2,3). При 80 0С суммарный выход продуктов составляет 80% при их соотношении 7/5. При 20 0С соотношение продуктов равно 1/1. Необычность этой реакции заключается в характере присоединения аллиьной группы – не традиционно линейном, а циклическом, и даже, с разрывом С-С – связи 2.
Строго говоря, взаимодействие НБН и аллилацетата не является содимеризацией. Аллилацетат выступает лишь как источник фрагмента С3Н4, присоединяющегося к НБН при помощи каталитического комплекса. Эта реакция является первым примером использования аллиловых эфиров органических кислот в подобных процессах и представляется интересным методом получения полициклических соединений.
Универсальность этого метода продемонстрирована в работах Джемилева и сотр.3 4 5 6, которые осуществили масштабное исследование этой реакции применительно к широкому кругу соединений НБН-ряда. Каталитическая система –Ni(асас) 2-АlEt3-Р(ОR) 3 весьма активна и достаточно селективна при получении экзо-метиленциклобутановых производных.
Каталитическое аллилирование НБН и НБН-производных - весьма сложный многопараметрический процесс. В системе, образованной большим количеством компонентов – металлоорганическими комплексами катализатора, фосфорорганическими соединениями, субстратами – (НБД) и сложными аллиловыми эфирами, а так же продуктами, возможно протекание как желательных, так и многочисленных побочных реакций, воздействующих на каталитическую систему и снижающих ее технологические показатели.
На состав продуктов существенное влияние оказывает природа растворителя. Так содимеризация АА с НБД наиболее успешно протекает в среде толуол – алифатический спирт (исключение составляет метанол) при различных соотношениях компонентов. В среде толуол – АсОН (1: 2) наблюдается изменение направления реакции в сторону образования продукта димеризации НБД, хотя меньшие количества АсОН, образующиеся за счет самой реакции, не влияют на активность и селективность каталитической системы 3.
Реакция чрезвычайно чувствительна к природе фосфорорганического лиганда. Наиболее активные катализаторы могут быть получены при использовании в качестве лигандов (i-PrO) 3P, (втор-BuO) 3P и (C6H11O) 3P 3. Каталитические системы на их основе проявляют активность в интервале 20 – 1200С.
Низкая активность каталитических систем на основе (MeO) 3P, (EtO) 3P, (PrO) 3P, (PhO) 3P и в особенности фосфинов может быть объяснена тем, что эти лиганды образуют достаточно прочные комплексы с Ni, препятствуя тем самым подходу к центральному атому катализатора и активированию НБН и АА.
На активность каталитических систем существенное влияние оказывает также температура. В работах 3 4 5 6 отмечается, что при 200С активность проявляют лишь каталитические системы, в которых в качестве лигандов используются (i-PrO) 3P, (втор-BuO) 3P и (C6H11O) 3P. И только при 800С высокие значения конверсии НБН и выхода продуктов достигаются для КС на основе (MeO) 3P, (EtO) 3P, (PrO) 3P, (PhO) 3P.
Строение аллилирующего агента – сложного аллилового эфира – не имеет решающего значения. Так, помимо аллилиацуетата с теми же результатами использованы аллилпропионат, аллилбутират. Аллилбензоат и аллилформиат. Однако, в случае последнего не удается добится высоких конверсий реагентов из-за разрушения каталитической системы. Аллиловый спирт, аллилгалогениды, простые аллиловые эфиры и тиоэфиры в реакции с НБН в данных условиях не вступают.
Природа восстановителя мало влияет на состав продуктов. Наиболее эффективными являются AlEt3, Al(i-Bu) 3, Mg(Bu) 2, и LiAlH4.
Стерические особенности субстратов, имеющих экзо-заместители в положениях 5 и 6 относительно внутрициклической двойной связи не оказывают существенного влияния на скорость циклоприсоединения. Содимеризация АА с подобными соединениями протекает строго избирательно и затрагивает только не замещенную двойную свзь. Однако, 5,6-эндо-заместители в зависимости от размера могут существенно затруднять реакцию вплоть до полной ее остановки. Процесс полностью блокируется также при наличии заместителя непосредственно у норборненовой двойной связи.
Сравнительное изучение каталитической активности для системы – Ni – (АА) 2 –AlEt3 – P(Oi-C3H7) 3 и индивидуального комплекса Ni (P(Oi-C3H7) 3) 4 указывают на существенные различия в их поведении.
Комплекс, выделенный в ходе реакции и охарактеризованный по продуктам распада, криоскопически имеет предположительный состав ((i-PrO) 3P) 3NiEt.
По-видимому, он является одним из интермедиатов в достаточно сложной цепочке превращений, приводящих к малоустойчивым каталитически активным гидридным (Ni-H) и кластерным (Ni-Ni) комплексам.
На основании кинетических и спектральных данных проведенных В.Р. Флидом и сотр., проведенных с 1980 по 2000 год 7 8 9 10 впервые был предложен был предложен механизм каталитического аллилирования НБН аллилиацетатом в присутствии никелевого катализатора.
В его основе лежат следующие положения:
Соединения никеля (0) являются четырехкоординационными с тетраэдрическим строением полиэдра. Это относится как к гомолигандным, так и смешанным с НБН никель - фосфитным комплексам.
Аллилацетат окислительно присоединяется к никелю, образуя пяти - и шестикоординационные комплексы.
Формирование продуктов аллилирования НБН осуществляется внутримолекулярно на моноядерном никелевом центре.
1. NiP4↔NiP3 + P
2. NiP3↔NiP2 + P
3. NiP2↔NiP + P
4. NiP + НБН↔Ni(НБН) + P
5. NiP2 + НБН↔NiP(НБН) + P
6. NiP3 + НБН↔NiP2(НБН) + P
7. NiP4 + НБН↔NiP3(НБН) + P
8. NiP4 + AA↔NiP4(AA)
9. NiP3 + AA↔NiP3(AA)
10. NiP2 + AA↔NiP2(AA)
11. NiP + AA↔NiP(AA)
12. NiP3(AA) + НБН↔NiP3(AA) (НБН)
13. NiP2(AA) + НБН↔NiP2(AA) (НБН)
14. NiP(AA) + НБН↔NiP(AA) (НБН)
15. NiP3(AA) (НБН) ↔S1 + AcOH + NiP3
16. NiP3(AA) (НБН) ↔S2 + AcOH + NiP3
17. NiP2(AA) (НБН) ↔S1 + AcOH + NiP2
18. NiP2(AA) (НБН) ↔S2 + AcOH + NiP2
19. NiP(AA) (НБН) ↔S1 + AcOH + NiP
20. NiP(AA) (НБН) ↔S2 + AcOH + NiP
21. P(O-iC3H7) 3 + AcOH↔H(O) P(O-iC3H7) 3 + C3H7Oac
Схема 1.2. Механизм каталитического аллилирования НБН.
P ≡ P(O-iC3H7) 3; НБН ≡ норборнен; АА ≡ аллилацетат; S1, S2 ≡ продукты аллилирования НБН.
К наиболее кинетически значимым стадиям меанизма следует отнести:
формирования в реакционном растворе комплексов (C3H5) PnNi(OAc), где n=2 или3. Эти комплексы доминируют в условиях реакции;
присоединение молекулы НБН к комплексу (C3H5) PnNi(OAc), сопровождающееся η3 – η1 – изомеризацией аллильного лиганда;
внедрение НБН по связи η1 – аллил – метал;
формирование никелациклических интермедиатов и их распад в резултате β-гидридного переноса с образованием продуктов аллилирования НБН и уксусной кислоты.

Рисунок 1.2. Заключительная часть механизма каталитического аллилирования НБН аллилиацетатом.
В реакции образуются изомеры исключительно экзо-строения, что связано с экзо-координацией молекул НБН-в комплексе.
β-гидридный перенос является завершающей и, как показывают проведенные исследования, лимитирующей стадией каталитического процесса. Следует отметить, что в стадии гидридного переноса могут участвовать атомы водорода как из аллильной группы аллилацетата, так и молекулы НБН.
Таким образом, в механизме протекания заключительного этапа наблюдается полная аналогия со стехиометрическими процессами, описанными в разделе 1.1.
Анализ изученных литературных данных 1 3 9 10 свидетельствует, что образование индивидуальных продуктов происходит из комплексов никеля, содержащих различное число фосфитных лигандов. Комплекс NiP3 ответственен за образование соединения II, а NiP2 – за продукт I. Этот факт играет важную роль при регулировании селективностию.
Серьезным препятствием на пути эффективного осуществления каталитического процесса и устойчивой работы катализатора является его дестабилизация одним из продуктов – уксусной кислотой. Образование последнего соединения происходит вэквивалентвых по отношению к продуктам аллилирования колличествах. Уксусная кислота переводит триизопрпилфосфит в неактивную форму, изменяя соотношение компонентов каталитической системы. В этой ситуации очень сложно добиться высоких технологических показателей процесса – селективности по индивидуальным продуктам и времени работы катализатора.
Проблема выведения уксусной кислоты из реакционной зоны представляется весьма непростой. Весьма перспективным в этом отношении представляется использование цеолитов типа NaA, которые являются абсолютно инертными по отношению к гомогенным никелевым комплексам 11 12. Применение цеолитов с диаметром пор 4Å позволяет весма эффективно и избирательно погощать уксусную кислоту (эффективный диаметр ≈3,8 Å).
Таким образом при использовании цеолитов количество каталитических циклов достигает 1,5 – 2 тыс.
Аллилирование соединений норборненового ряда.
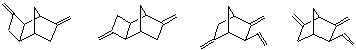
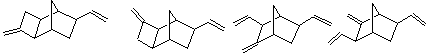
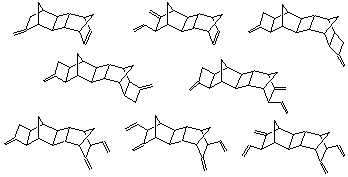
Закономерности, выявленные при каталитическом аллилировании НБН, справедливы для многочисленных НБН-производных 3 10 Киузоли 85 (табл.1.2).
Варьирование двух параметров - соотношения P/Ni и температуры - позволяет получать метилен циклобутановые соединения типа I с селективностью 80-95%, а метилен-винильные производные типа II – с селективностью 75-85%.
В реакцию вступают только НБН-производные с незамещенной двойной связью. Соединения, имеющие несколько ненасыщенных связей различной природы, участвуют в реакции только с использованием двойной НБН-связи.
Пространственный фактор оказывает влияние на скорость процесса, но соотношение изомеров маю от него зависит. Наиболее активны норборнены с неэкранированной внутри циклической двойной связью, имеющие экзо-заместители в положениях 5 или 6 НБН-кольца. Активность эндо-замещенных производных в реакции несколько ниже.
Соединения, имеющие две изолированные НБН-двойные связи последовательно аллилируются по каждой из них, причем активность в каждой из стадий практически неизменна. Здесь возможно образование большого количества изомеров, но варьирование вышеуказанных параметров позволяет преимущественно получать два из них.
Сопоставляя закономерности протекания стехиометрического (раздел 4.6) и каталитического аллилирования, можно отметить ряд качественных аналогий по составу и строению продуктов.
Как правило, в обеих реакциях образуются одни и те же соединения. В каталитическом процессе полностью отсутствуют изомеры эндо-строения, тогда как в стехиометрическом варианте такие соединения образуются, хотя и в незначительных количествах.
Каталитический вариант в отличие от стехиометрического позволяет направленно воздействовать на соотношение изомеров.
Механизм протекания ключевых стадий полностью аналогичен.
Таблица 1.2
Продукты аллилирования замещенных норборненов.
| Исходное соединение | Продукты |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Подобные работы: