Свойства жидкостей
Национальный университет Узбекистана
Физический факультет
РефератСвойства жидкостей
Составил: студент 1 курса
Овсянников А. В.
Ташкент – 2004
- Объемные свойства жидкостей
Молекулы в жидкостях находятся близко друг к другу, примерно на расстояниях равных размерам самих молекул. Это является причиной высокого молекулярного ван-дер-ваальсового давления, которое равно 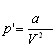 . Для воды, например, он равен около 11000 атм. Удельный объем жидкостей в тысячи раз меньше чем газов, следовательно, отношение
. Для воды, например, он равен около 11000 атм. Удельный объем жидкостей в тысячи раз меньше чем газов, следовательно, отношение ![]() в жидкостях в миллионы раз больше, чем в газах. Поэтому можно пренебречь внешним давлением, и уравнение Ван-дер-Ваальса примет вид
в жидкостях в миллионы раз больше, чем в газах. Поэтому можно пренебречь внешним давлением, и уравнение Ван-дер-Ваальса примет вид
![]()
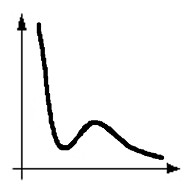
Большой величиной молекулярного давления объясняется ничтожно малая сжимаемость жидкостей. Это сразу видно из уравнения кривой Ван-дер-Ваальса, на которой жидкому состоянию соответствует участок AB (см. рис. 1). Коэффициент сжимаемости χ жидкости – относительное изменение объема dV при изменении давления на единицу т.е.
Опыт показывает, что коэффициент сжимаемости большинства жидкостей лежит в пределах от 10-4 до 10-5 ![]() .
.
Коэффициент сжимаемости жидкости зависит от давления. Он возрастает с повышением температуры. К этому результату можно прийти и опытным путем и исходя из уравнения Ван-дер-Ваальса. Поскольку это уравнение связывает температуру, объем и давление, то из него можно вычислить величину ![]() . При расчете необходимо учитывать, что постоянные a и b на самом деле зависят от температуры. Совокупность опытных данных позволила получить эмпирическую формулу для коэффициента сжимаемости жидкости:
. При расчете необходимо учитывать, что постоянные a и b на самом деле зависят от температуры. Совокупность опытных данных позволила получить эмпирическую формулу для коэффициента сжимаемости жидкости:
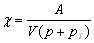
где A – некоторая функция, возрастающая с температурой, p – внешнее давление и pT – давление, связанное с силами Ван-дер-Ваальса (a/V2) при температуре T. Эта формула показывает, что коэффициент сжимаемости растет с повышением температуры и уменьшается с ростом давления.
Среди всех жидкостей наибольшей сжимаемостью обладает жидкий гелий, у которого при давлении в несколько атмосфер коэффициент χ равен ![]() . Коэффициент сжимаемости воды равен
. Коэффициент сжимаемости воды равен ![]() , а ртути –
, а ртути –![]()
![]() .
.
Тепловое расширение вещества характеризуется коэффициентом объемного расширения
![]() ,
,
т.е. относительным изменением объема V при изменении температуры T на 1 К.
Числовые значения коэффициента α сильно зависят от температуры и давления. Для различных жидкостей значения α при одинаковых температурах могут меняться весьма значительно. Так, например, для воды ![]() , для бензола
, для бензола ![]() , для жидкой углекислоты
, для жидкой углекислоты ![]() , глицерина
, глицерина ![]() и т.д. При повышении температуры α сильно возрастает. Так для жидкой углекислоты при повышении температуры от 0° до 20° коэффициент теплового расширения возрастает вдвое. Увеличение давления несколько снижает значение α.
и т.д. При повышении температуры α сильно возрастает. Так для жидкой углекислоты при повышении температуры от 0° до 20° коэффициент теплового расширения возрастает вдвое. Увеличение давления несколько снижает значение α.
Вода обладает аномальным тепловым расширением. В интервале от 0° до 3,98° коэффициент α отрицателен: при нагревании объем воды уменьшается и наибольшей плотности вода достигает при 3,98° C. При этой температуре α = 0.
Причиной этого явления является то, что молекулы воды имеют различный состав: не только H2O, но 2H2O и 3H2O. Относительные количества этих молекул меняются с температурой и давлением.
- Теплоемкость жидкостей
Внутренняя энергия жидкостей определяется не только кинетической энергией тепловых движений частиц, но и их потенциальной энергией взаимодействия. Поэтому закономерности, полученные для теплоемкостей идеальных газов из уравнений кинетической теории, не могут быть справедливы для жидкостей.
Опыт показывает, что теплоемкость жидкостей зависит от температуры, причем вид зависимости у разных жидкостей различный. У большинства из них теплоемкость с повышением температуры увеличивается, но есть и такие у которых, наоборот, - уменьшается. У некоторых жидкостей теплоемкость с повышением температуры сначала падает, а затем, пройдя через минимум, начинает расти. Такой ход теплоемкости наблюдается у воды. Жидкости с большим молекулярным весом обычно имеют большие значения теплоемкостей. Особенно это проявляется у органических жидкостей.
У жидкостей, как и газов, следует различать теплоемкость при постоянном объеме и при постоянном давлении. Разность молярных теплоемкостей равна Cp – CV равна работе расширения pdV ( p – молекулярное давление ) моля жидкости при его нагревании на один градус, поэтому численное значение этой разности зависит от значения коэффициента объемного теплового расширения жидкости. В отличие от идеальных газов значение Cp - CV у жидкостей не равно постоянной R, а может быть и больше и меньше в зависимости от значения коэффициента объемного расширения и от величины внутренних сил взаимодействия частиц жидкости, против которых совершается работа расширения (давление p в выражении pdV связано именно с этими силами).
Так, у жидкого аргона при 140 К теплоемкость ![]() , а
, а ![]() и, следовательно
и, следовательно ![]() . У воды же при температуре около 0° C теплоемкость
. У воды же при температуре около 0° C теплоемкость ![]() , а
, а ![]() , так что
, так что ![]() .
.
Таким образом, численные значения теплоемкостей жидкостей могут быть самыми разнообразными. Исключение составляют жидкие металлы, у которых молярная теплоемкость обычно близка к значению ![]() .
.
- Явления переноса в жидкостях
В жидкостях, как и в газах, наблюдаются явления диффузии, теплопроводности и вязкости. Но механизм этих процессов в жидкостях иной, чем в газах.
В отличие от газов, в жидкостях отсутствует понятие длины свободного пробега. Это связано с тем, что в жидкостях среднее расстояние между молекулами такого же порядка, как и размеры самих молекул. Молекулы жидкости могут совершать лишь малые колебания в пределах, ограниченных межмолекулярными расстояниями.
Такие колебания молекул время от времени сменяются скачками на некоторое расстояние δ, происходящими из-за получения молекулой в результате флуктуации избыточной энергии от соседних молекул. Колебания, сменяющиеся скачками, – и есть тепловые движения молекул жидкости.
Диффузия
Для явления диффузии в жидкости справедлив закон Фика. Он гласит:
![]() ,
,
где I – диффузионный поток в направлении оси X, D – коэффициент диффузии, а ![]() - градиент концентрации по оси X.
- градиент концентрации по оси X.
Обозначим время между скачками молекул через t, тогда величина ![]() - скорости молекулы. Это дает возможность сравнить
- скорости молекулы. Это дает возможность сравнить ![]() со средней длинной свободного пробега, а
со средней длинной свободного пробега, а ![]() - со средней скоростью молекул. Тогда по аналогии с идеальными газами коэффициент диффузии (точнее самодиффузии) жидкости равен:
- со средней скоростью молекул. Тогда по аналогии с идеальными газами коэффициент диффузии (точнее самодиффузии) жидкости равен:
![]() .
.
Коэффициент самодиффузии сильно зависит от температуры, т.е. с повышением температуры он увеличивается.
Выражение коэффициента диффузии можно переписать в виде
![]() ,
,
где ![]() , причем ν - частота вышеописанных колебаний, а w – энергия, необходимая для скачка молекулы, называемая энергией активации молекулы.
, причем ν - частота вышеописанных колебаний, а w – энергия, необходимая для скачка молекулы, называемая энергией активации молекулы.
Численное значение коэффициента диффузии у жидкостей много меньше чем у газов. Например коэффициент диффузии NaCl в воде равен 1,1·10-9 м2/с, в то время как для диффузии аргона в гелий он равен 7·10-5 м2/с.
Вязкость
Внутреннее трение жидкостей возникает при движении жидкости из-за переноса импульса в направлении, перпендикулярном к направлению движения. Перенос импульса из одного слоя в другой осуществляется при скачках молекул, о которых говорилось выше.
Очевидно, что жидкость будет тем менее вязкой, чем меньше время t между скачками молекул, и значит, чем чаще происходят скачки. Исходя из этого, можно написать выражение для коэффициента вязкости, называемого уравнением Френкеля – Андраде:
![]() .
.
Множитель C, входящий в это уравнение зависит от дальности скачка ![]() , частоты колебаний ν и температуры. Однако температурный ход вязкости определяется множителем ew/kT. Как следует из этой формулы, с повышением температуры вязкость быстро уменьшается.
, частоты колебаний ν и температуры. Однако температурный ход вязкости определяется множителем ew/kT. Как следует из этой формулы, с повышением температуры вязкость быстро уменьшается.
Теплопроводность
Теплопроводность в жидкостях имеет место при наличии градиента температуры. При этом энергия в жидкостях передается в процессе столкновения колеблющихся частиц. Частицы с более высокой энергией совершают колебания с большей амплитудой, и при столкновениях с другими частицами как бы раскачивают их, передавая им энергию. Такой механизм передачи энергии не обеспечивает ее быстрого переноса. Поэтому теплопроводность жидкостей очень мала.
Например, коэффициент теплопроводности этилового спирта составляет 1,76 Вт/м·К. Исключение составляют жидкие металлы, коэффициенты теплопроводности которых близки к значениям для твердых металлов. Это объясняется тем, что тепло в жидких металлах переносится не только вместе с передачей колебаний от одних частиц к другим, но и при помощи электронов, которые есть в металлах, но отсутствуют в других жидкостях.
- Парообразование и кипение
Испарение
В поверхностном слое и вблизи поверхности жидкости действуют силы, которые обеспечивают существование поверхности и не позволяют молекулам покидать объем жидкости. Благодаря тепловому движению некоторая часть молекул имеет достаточно большие скорости, чтобы преодолеть силы, удерживающие молекулы в жидкости, и покинуть жидкость. Это явление называется испарением. Оно наблюдается при любой температуре, но его интенсивность возрастает с увеличением температуры.
Если покинувшие жидкость молекулы удаляются из пространства вблизи поверхности жидкости, то, в конце концов, вся жидкость испарится. Если же молекулы, покинувшие жидкость не удаляются, то они образуют пар. Молекулы пара, попавшие в область вблизи поверхности жидкости, силами притяжения втягиваются в жидкость. Этот процесс называется конденсацией.
Таким образом, в случае неудаления молекул скорость испарения уменьшается со временем. При дальнейшем увеличении плотности пара достигается такая ситуация, когда число молекул, покидающих жидкость за некоторое время, будет равно числу молекул, возвращающихся в жидкость за то же время. Наступает состояние динамического равновесия. Пар в состоянии динамического равновесия с жидкостью называется насыщенным.
С повышением температуры плотность и давление насыщенного пара увеличиваются. Чем выше температура, тем большее число молекул жидкости обладает энергией, достаточной для испарения, и тем большей, должна быть плотность пара, чтобы конденсация могла сравняться с испарением.
Кипение
Когда при нагревании жидкости достигается температура, при которой давление насыщенных паров равно внешнему давлению, устанавливается равновесие между жидкостью и ее насыщенным паром. При сообщении жидкости дополнительного количества теплоты происходит немедленное превращение соответствующей массы жидкости в пар. Этот процесс называется кипением.
Температурой кипения является та температура, при которой давление насыщенных паров становится равным внешнему давлению. При увеличении давления температура кипения увеличивается, а при уменьшении - уменьшается.
По причине изменения давления в жидкости с высотой ее столба, кипение на различных уровнях в жидкости происходит, строго говоря, при различной температуре. Определенную температуру имеет лишь насыщенный пар над поверхностью кипящей жидкости. Его температура определяется только внешним давлением. Именно эта температура имеется в виду, когда говорят о температуре кипения.
Количество тепла, которое необходимо подвести, для того чтобы изотермически превратить в пар определенное количество жидкости, при внешнем давлении, равном давлению ее насыщенных паров, называется скрытой теплотой парообразования. Обычно эту величину соотносят к одному грамму, или одному молю. Количество теплоты, необходимое для изотермического испарения моля жидкости называется молярной скрытой теплотой парообразования. Если эту величину поделить на молекулярный вес, то получится удельная скрытая теплота парообразования.
Литература:
- А. К. Кикоин, И. К. Кикоин, Молекулярная физика, «Наука», 1976.
- Телеснин Р. В., Молекулярная физика, «Высшая школа», 1973.
- Матвеев А. Н., Молекулярная физика, «Высшая школа», 1987.