Метод радиоавтографии в биологии
Реферат:
Метод радиоавтографии
Радиоавтография, определение, история.
Метод радиоавтографии основан на введении в исследуемый объект соединения, "меченого" радиоактивным атомом и выявлении места его включения путем фотографической регистрации излучения. Основой получения изображения является воздействие ионизирующих частиц, образующихся при распаде радиоактивного атома, на ядерную фотоэмульсию, содержащую кристаллы галоидного серебра.
Открытие метода радиоавтографии напрямую связано с открытием явления радиоактивности. В 1867 году было опубликовано первое наблюдение о влиянии солей урана на галогениды серебра (Niepce de St.Victor). В 1896 году Генри Беккерель наблюдал засвечивание фотопластинки солями урана без предварительной экспозиции на свету. Этот эксперимент считается моментом открытия явления радиоактивности. Радиоавтографию применительно к биологическому материалу впервые использовали Лакассань и Латтье (Lacassagne, Lattes 1924) в 20-х годах прошлого века; гистологический блок от различных органов животных после введения им изотопов прижимали плоской стороной к рентгеновской пластинке и экспонировали. Заранее получали гистологический срез и подвергали стандартной процедуре окраски. Полученный автограф изучали отдельно от среза. Этот метод позволяет оценить интенсивность включения изотопа в биологический образец. В сороковых годах Леблон использовал радиоавтографию для демонстрации распределения изотопа иода в срезах щитовидной железы (Leblond C.P. 1943).
Первые попытки сочетать радиоавтографию с электронной микроскопией были сделаны в 50-е годы (Liquir-Milward, 1956). Электронно-микроскопическая радиоавтография представляет собой частный случай обычной радиоавтографии, при котором также подсчитываются зерна серебра и учитывается их распределение. Особеннось метода состоит в применении очень тонкого слоя эмульсии. В настоящее время достигнуто разрешение около 50 нм, что в 10-20 раз выше в сравнении со световой микроскопией.
В настоящее время метод радиоавтографии дополнен возможностью автоматической оценки количества зерен серебра с помощью видеоанализаторов. Часто для усиления сигнала метки (как правило это изотопы с высокими энергиями) применяются различные виды сцинтиляторов, нанесенные на пластины (усиливающий экран с фосфорным покрытием), или импрегнированные в эмульсию (PPO) – в таком случае излучение фотонов засвечивает обычную фотопластину или фотопленку.
Фотографический принцип получения изображения, фотоэмульсии
В радиографическом исследовании роль детектора ядерных распадов выполняет фотоэмульсия, в которой при прохождении ионизирующей частицы остается скрытое изображение, выявляемое затем в процессе проявки, аналогично обработке обычной фотопленки.
Фотоэмульсия представлет из себя взвесь микрокристаллов галоидного серебра в желатине. Микрокристаллы имеют дефекты в структуре, называемые центрами чувствительности. Согласно модели Гэрни-Мотта эти нарушения ионной решетки кристалла способны захватывать электроны, высвободившиеся при прохождении альфа- или бета-частицы в зоне проводимости кристалла, в результате чего ион превращается в атом. Образовавшееся скрытое изображение может быть выявлено с помощью процедуры, в результате которой активированные кристаллы галоидного серебра превращаются в зерна металлического серебра (этот процесс называется химической проявкой). В качестве проявителя может быть использован любой агент с достаточной восстанавливающей активностью (типично в фотографии и авторадиографии используются метол, амидол или гидрохинон). После проявления экспонированных кристаллов остальные микрокристаллы галоидного серебра удаляют из эмульсии при помощи фиксатора (обычно - гипосульфит). Ядерные фотоэмульсии характеризуется разрешающей способностью (зернистостью) и чувствительностью. Первая определяется размером микрокристаллов соли серебра и обратно пропорциональна последней. Фотоэмульсия характеризуется пониженной чувствительностью к видимому свету, но работа с ней, тем не менее, должна производится в темноте, чтобы исключить появление артефактов.
Эмульсия может наносится на препарат в виде готовой пленки с подложкой или погружением препарата в разогретую жидкую эмульсию – таким образом получается тонкий равномерный слой, который проявляется обычным способом. Перед нанесением эмульсии для световой микроскопии препарат обычно окрашивают требуемой гистологической окраской, но более бледно, чем обычно, чтобы сделать возможным подсчет зерен серебра на всех участках. Определенное время препарат экспонируют, затем проявляют.
Изотопы, используемые в радиоавтографии.
В радиоавтографии в зависимости от целей исследования и доступных материалов возможно применение различных изотопов. Изображение, создаваемое ионизирующей частицей на ядерной фотоэмульсии зависит от энергии частицы и типа ее взаимодействия с веществом.
Альфа-частицы, испускаемые одинаковыми радиоактивными ядрами обладают одинаковой энергией (E) и одинаковой длиной пробега (R), связанными следующим соотношением:
R = kE3/2
Где k – константа, характеризующая среду, в которой распространяются частицы. Величина пробега частиц в серде определяется ее плотность и элементарным составом. Соотношение Брегга-Климена позволяет по величине пробега альфа-частиц в воздухе (R0 ) оценить пробег в веществе с атомной массой A и плотностью d:
R=0,0003 ( R0 / d ) A1/2
Поскольку ионизирующая способность альфа-частиц очень высока, это облегчает фотографическую регистрацию распределения изотопа, а так же позволяет использовать для регистрации неэмульсионные материалы. След альфа-частиц, испускаемых одним источником, на автографах выглядит как пучок прямолинейных отрезков, обычно длиной 15-50 мкм, исходящих из одной точки, что позволяет точно локализовать участок включения радиоактивной метки. Однако, альфа-частицы испускаются изотопами с большими атомными номерами, что ограничивает возможность их применения в качестве биологической метки.
Треки альфа-частиц часто наблюдаются в гистологических радиовтографах как артефакт – результат собственного излучения изотопов, находящихся в предметном стекле.
Бета излучение характеризуется непрерывным спектром начальной энергии частиц – от нуля до определенной для каждого изотопа E max. Формы спектра существенно отличаются. Так, наиболее вероятная энергия частиц, излучаемых тритем составляет 1/7 от E max, 14C – около ¼, 32P – около 1/3. Максимальная энергия бета-излучения различных изотопов меняется в пределах от 18 кэВ до 3.5 МэВ – в гораздо более широких пределах, чем альфа излучения. Как правило, максимальная энергия выше у короткоживущих изотопов.
Прохождение бета-частиц и моноэнергетических электронов через вещество сопровождается двумя основными типами взаимодействия. При взаимодействии с орбитальным электроном частица может передать ему энергию, достаточную для ионизации атома (удаления электрона с орбиты). В редких случаях эта энергия настолько велика, что можно наблюдать трек освобожденного электрона. Из-за равенства масс частицы и электрона происходит отклонение от первоначального движения. Взаимодествие второго типа , с атомными ядрами, приводит к возникновению тормозного рентгеновского излучения. Хотя последнее и не регистрируется эмульсией, акт взаимодейтсвия частицы с ядром может быть обнаружен по резкому излому траектории.
Многократное взаимодействие с орбитальными электронами приводит к искривлению траектории, которая обычно выглядит как извилистая линия, особенно в конечной части, когда скорость частицы падает, а ионизирующая способность возрастает. Длина траектории заметно превышает расстояние от начальной до конечной точки трека – пробег. По этой причине даже для моноэнергетических электронов характерно наличие спектра пробегов, ограниченного сверху R max, харакерным для данного излучения. Из-за более низких ионизационных потерь бета частицы регистрируются с большими сложностями, чем альфа-частицы. Они не образуют сплошных треков (кроме самого мягкого излучения трития – однако в этом случае мала вероятность прохождения более чемп через один кристалл эмульсии), плотность и число проявленных кристаллов варьируют в различных пределах. Пробег бета-частицы в другом элементе может быть оценен по формуле:
R = RA1 (Z/A)A1/ (Z/A)
В широком диапазоне значений Emax максимальный пробег связан с максимальной энергией соотношением:
Rm = 412 Emax1.265 – 0,0954 ln Emax
Различие в пробегах, ионизационной способности и плотности проявленных эмульсионных кристаллов у частиц с различной энергией может быть использовано для дискриминации распределения элементов, эсли их изотопы существенно отличаются по E max, как в случае с тритием и 14С. Дискриминацию распределения двух изотопов осуществляют с помощью нанесения на образец двух эмульсионных слоев, первый слой регистрирует преимущественно мягкое излучение, второй – жесткое. Согласно некоторым работам различные изотопы могут быть надежно выделены по размеру проявленных эмульсионных кристаллов - кристаллы, затронутые бета-частицей трития, обладающей большей ионизационной способностью, имеют большие размеры.
Электроны внутренней конверсии образуются при поглощении гамма кванта с очень низкой энергией излучения и удалении электрона с внутренней оболочки атома. Эти электроны подобны мягким бета-частицам, но в отличие от последних являются моноэнергетическими. Наличие электронов внутренней конверсии позволяет использовать такие изотопы как 125I.
В настоящее время чаще всего используются изотопы, излучающие бета-частицы. Как правило для метки в гистологических исследованиях используется тритий. Первые автографы с использование трития были изготовлены еще в 50-е годы (Fitzgerald et al. 1951), однако широкое его применение началось после того, как в Брукхэвенской лаборатории был получен меченый тритием тимидин. Поскольку водород входит в состав всех органических веществ, то, используя тритий, можно получать самые разные соединения, несущие радиоактивную метку. Чем меньше энергия испускаемой частицы, тем короче трек, оставляемый ей при движении в фотоэмульсии и тем точнее можно локализовать расположение меченого атома. Длина пробега бета-частиц трития около 1-2 мкм, наиболее вероятная энергия 0,005 МэВ, а трек состоит в большинстве случаев из одного зерна серебра, что позволяет локализовать источник излучения не только в относительно крупных клеточных структурах, таких как ядро, но и в отдельных хромосомах.
Введение "меченых" метаболитов в организм позволяет проследить включение изотопа в клетки тканей животного, что дает возможность исследовать самые разные биохимические процессы в живом организме.
Получение абсолютных данных – концентрации меченого вещества в изучаемом объекте редко бывает целью радиоавтографического исследования, для этого необходимо знание ряда условий, определение которых затруднено. Поэтому количественные радиоавтографические исследования обычно проводят путем сравнения концентрации зерен серебра над исследуемым объектом и контролем, при этом контрольные данные удобно принимать за единицу, или 100%.
Характеристики некоторых изотопов, используемых
в радиоавтографии биологических объектов
Изтоп | Период полураспада | Частица | Максимальная энергия излучения |
3H | 12.35 лет | β- | 0.019 МэВ |
14C | 5730 лет | β- | 0.155 МэВ |
35S | 87.4 дня | β- | 0.176 МэВ |
32P | 14.3 дня | β- | 1.709 МэВ |
45Ca | 164 дня | β- | 0.250 МэВ |
Бета-частицы радиоактивного фосфора способны пролетать в ядерной эмульсии расстояния до нескольких миллиметров, трек состоит из десятков редко расположенных частиц серебра – так, радиоактивный фосфор может быть использовани только для изучения распределения изотопа в тканях, локализацию в отдельных клеточных структурах установить невозможно.
Радиоактивные сера и углерод могут быть использованы для локализации изотопа в отдельных клетках, при условии того, что они крупные или расположены на достаточном расстоянии друг от друга, что может быть достигнуто в мазках крови или клеточных суспензиях.
Разрешающая способность и погрешности метода, ошибки метода.
Под разрешающей способностью понимают степень точности с которой можно определить локализацию в препарате радиоактивного вещества («метки»). Разрешающая способность метода в данном случае ограничена двумя факторами.
Геометрическая ошибка – в связи с тем, что испускаемая частица может быть направлена под любым углом к поверхности фотослоя. Следовательно, зерно серебра в фотослое может быть расположено не точно над радиоактивным атомом, а более или менее смещено в зависимости от направления движения частицы и длины пробега (энергии).
Фотоошибка возникает в связи с тем, что зерно серебра, состоящее из тысяч атомов металла намного больше, чем радиоактивный атом. Таким образом, о локализации меньшего объекта приходится судить исходя из положения большего.
При использовании трития, характеризующегося малой энергией (пробегом) испускаемых частиц и ядерных фотоэмульсий с низкой зернистостью разрешающая способность метода радиоавтографии лежит в пределах разрешающей способности оптических систем – 1 мкм. Таким образом, эти ошибки не имеют существенного влияния на получаемый результат.
Для достижения лучшего разрешения необходимо уменьшать толщину среза, слоя эмульсии и расстояние между ними. Препарат следует немного недоэкспонировать.
Эффект автоабсорбции: Число зерен серебра зависит от степени поглощения излучения клеточными структурами, благодаря малому пробегу и малой энергии бета-частиц, их абсорбция в тканях достаточно велика, что может приводить к потере метки, поэтому важное значение приобретает вопрос о толщине срезов. Показано, что число зерен серебра пропорционально радиоактивности ткани только при толщине среза не более 5 мк.
Относительное число бета-частиц, прошедших сквозь слой поглотителя толщиной х может быть оценено по закону Бэра –
Nx/N0 = e -μ x
Где μ - коэффициент поглощения (величина, обратная толщине слоя, при прохождении которого число частиц уменьшается в e раз. Величину коэффициента поглощения можно приближенно оценить по величине Rm (максимальный пробег), известной для всех изотопов, с помощью соотношения μ Rm = 10, справедливого для не слишком жестких излучений.
Если в слое единичной толщины в единицу времени возникает n частиц, движущихся к поверхности, то в образце толщиной х поверхности достигнет N частиц:
N = 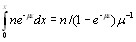
Фон и артефакты: Ошибку в измерения могут вносить так же механические воздействия – царапины, трещины эмульсии, ведущие к образованию скрытого изображения и фоновое излучение, которое необходимо учитывать при обработке радиоавтографов. Фон учитывают подсчетом числа зерен серебра на пустом участке препарата. Ошибки так же вносятся в результате гистологической обработки срезов – проводки по спиртам (дегидратации), заключения в парафин, окраски. Эти процедуры могут влиять на размеры и соотношения клеточных структур.
Радиационный эффект меченых метаболитов: Благодаря малой энергии излучения тритий вызывает в клетке значительную ионизацию, намного превышающую радиационный эффект бета-частиц углерода. Вследствие этого при продолжительном действии меченого соединения например 3H-тимидина происходит разрушение и гибель клеток, приводящие к остановке роста тканей. В первую очередь нарушается сперматогенез. Имеются данные о мутагенном и канцерогенном действии меченых метаболитов. Наблюдаемые цитологические изменения заключаются в нарушении прохождения клетками митотического цикла, изменении плоидности клеток и появлении хромосомных аберраций. Но, по-видимому, повреждающее действие изотопа на клетки мождет заметным образом сказываться на результатах исследования лишь в условиях длительного эксперимента.
Количественная оценка радиоактивности
Как правило, в эксперименте определяют не абсолютное, а относительное количество включившегося изотопа. Степень включения метки можно оценить двумя способами – денситометрически – что более применимо к макроавтографам и прямым подсчетом зерен серебра над объектами. Эта трудоемкая процедура в настоящее время может быть выполнена с помощью компьютера. Цифровой снимок гистологического препарата обрабатывается специальным програмным обеспечением, с целью автоматически выделить на нем клетки и клеточные структуры и подсчитать косличество зерен серебра. Если встает вопрос о количественной оценке – необходимо привлекать понятие эффективности. Чаще всего под эффективностью понимают число зерен серебра, образующихся при регистрации одного радиоактивного распада. На эффективность метода влияют многие факторы, в первую очередь толщина объекта и эмульсии.
В исследованиях с помощью сцинтиляционного счетчика была найдена высокая корреляция между средним числом распадов в минуту и количсетвом зерен серебра. По данным Ханта (Hunt, Foote, 1967) образование одного зерна в применявшейся в эксперименте эмульсии соответствует 5.8 радиоактивных распадов, т.е эффективность метода составляет 17.8%.
Для количественной оценки трития в макроскопических препаратах могут быть использованы образцы со стандартной активностью, которые монтируются на том же автографе.
Точна оценка радиоактивности сравниваемых биологических объектов очень сложна.
Примеры исследований методом авторадиографии
Классический пример радиоавтографического исследования – это работа по изучению накопления 32P в ДНК клеток корня конского боба (Howard, Pelc, 1953). В этом эксперименте было впервые показано деление митотического цикла на четыре периода (митоз - M, G1- пресинтетический период, S – синтез ДНК, премитотический период G2), что период синтеза ДНК занимает ограниченную часть интерфазы, будучи отделен во времени от начала и окончания митоза. Данные Говард и Пелка позднее нашли подтверждение в более точных экспериментах с применением спецефического предшественника ДНК – 3H-тимидина.
Методы оценки синтеза белка. Наиболее распространенными предшественниками для оценки общего белкового синтеза в радиоавтографических исследованиях служат 3H-лейцин, 3H-метионин, 3H-фенилаланин. Например, с использованием лейциновой метки изучался синтез общего белка в головном мозге крыс первых недель постнатального развития (Pavlik, Jakoubek, 1976). Для изучения синтеза гистонов и их влияния на регуляцию транскрипции используют основные аминокислоты 3H-лизин и 3H-аргинин, для изучения синтеза кислых белков - 3H-триптофан. Плотность включения аминокислотной метки соответствует интенсивности синтеза белка, а следовательно отражает функциональную активность нейрона. Радиоавтографический метод позволяет сравнивать особенности синтеза белка в различных тканях животных при экспериментальном воздействии, позволяет проследить динамику изменений на уровне отдельных типов клеток и клеточных структур (ядро, тело клетки, отростки нейрона – аксональный транспорт).
Радиоавтографическим методом также были получены данные о полуконсервативном механизме редупликации хромосом, асинхронность синтеза ДНК в разных участках хромосомы, изучение организации хромосом.
В настоящее время радиоавтографический метод часто используется для изучения мозга в работах с использованием радиолигандов к определенным рецепторам. Таким образом построены карты распределения различных рецепторов в структурах мозга животных и человека.
Радиоавтографический метод также используется для визуализации гелей в биохимии и в сочетании с иммунологическими методами (РИА).
Использованная литература:
1.Епифанова О.И. и др. Радиоавтография М., «Высш.школа», 1977
2.Саркисов Д.С. Перов Ю.Л. Микроскопическая техника М.: «Медицина», 1996
3.Rogers A.W. Practical autoradiography, Amersham UK, 1982
4.Бокштейн С.З. Гинзбург С.С. и др. Электронно-микроскопическая авторадиография в металловедении М., «Металлургия»